早教吧作业答案频道 -->化学-->
氯化铁和高铁酸钾都是常见的水处理剂.如图为制备氯化铁及进一步氧化制备高铁酸钾的工艺流程.请回答下列问题:(1)请用离子方程式表示下列反应原理.①用惰性电极电解饱和食盐水
题目详情
氯化铁和高铁酸钾都是常见的水处理剂.如图为制备氯化铁及进一步氧化制备高铁酸钾的工艺流程.
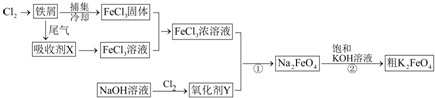
请回答下列问题:
(1)请用离子方程式表示下列反应原理.
①用惰性电极电解饱和食盐水___.
②氯化铁做净水剂___.
(2)吸收剂X的化学式为___;氧化剂Y的化学式为___.
(3)碱性条件下反应①的离子方程式为___.
(4)已知25°C时Fe(OH)3的Ksp=4.0×10-38,反应①后的溶液中c(Fe3+)=4.0×10-5mol/L,为获得较纯净的Na2FeO4则需调整pH至少为___时会生成Fe(OH)3沉淀.
过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品.该反应的化学方程式为2KOH+NaFeO4=K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因___.
(5)K2FeO4在水溶液中易发生反应:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O3↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用___(填序号).
A.H2O
B.稀KOH溶液、异丙醇
C.NH4Cl溶液、异丙醇
D.Fe(NO3)3溶液、异丙醇.

请回答下列问题:
(1)请用离子方程式表示下列反应原理.
①用惰性电极电解饱和食盐水___.
②氯化铁做净水剂___.
(2)吸收剂X的化学式为___;氧化剂Y的化学式为___.
(3)碱性条件下反应①的离子方程式为___.
(4)已知25°C时Fe(OH)3的Ksp=4.0×10-38,反应①后的溶液中c(Fe3+)=4.0×10-5mol/L,为获得较纯净的Na2FeO4则需调整pH至少为___时会生成Fe(OH)3沉淀.
过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品.该反应的化学方程式为2KOH+NaFeO4=K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因___.
(5)K2FeO4在水溶液中易发生反应:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O3↑.在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用___(填序号).
A.H2O
B.稀KOH溶液、异丙醇
C.NH4Cl溶液、异丙醇
D.Fe(NO3)3溶液、异丙醇.
▼优质解答
答案和解析
(1)①用惰性电极电解饱和食盐水时,阳极上氯离子放电,阴极上氢离子放电,同时溶液中还生成氢氧化钠,所以电池反应式为2NaCl+2H2O
2NaOH+H2↑+Cl2↑,离子反应方程式为:2Cl-+2H2O
Cl2↑+H2↑+2OH-,
故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-;
②氯化铁做净水剂是因为Fe3+水为Fe(OH)3胶体的缘故,原理为Fe3++3H2O⇌Fe(OH)3(胶体)+3H+,
故答案为:Fe3++3H2O⇌Fe(OH)3(胶体)+3H+;
(2)吸收剂X的与Cl2反应的产物是FeCl3,X是FeCl2;Cl2与氢氧化钠反应生成NaClO和NaCl,其中NaClO能做氧化剂,所以Y为NaClO,
故答案为:FeCl2;NaClO;
(3)碱性条件下根据反应物和产物可知,反应①的离子方程式为3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O;
故答案为:3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O;
(4)25℃时Fe(OH)3的Ksp=4.0×10-38,反应Ⅱ后的溶液中c(Fe3+)=4.0×10-5mol/L,Ksp=c(Fe3+)×c3(OH-),c3(OH-)=
=10-33;c(OH-)=10-11mol/L
c(H+)=
=10-3mol/L,铁离子沉淀的溶液PH=3;过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品.该反应的化学方程式为2KOH+Na2FeO4 =K2FeO4+2NaOH,K2FeO4的溶解度比Na2FeO4小而溶液中K+、FeO42-的浓度比较大;K2FeO4在水溶液中易发生反应:4FeO42-+10H2O═4Fe(OH)3+8OH-+3O2↑,
故答案为:3;K2FeO4溶解度小,析出晶体,促进反应进行;
(5)洗涤剂的选择要求:要对K2FeO4水解能起到抑制作用的试剂,在选项中,A能让K2FeO4水解,B中稀KOH溶液显碱性,对K2FeO4水解能起到抑制作用,C和D中的铵根和三价铁离子易水解,且水解后显酸性,对K2FeO4水解能起到促进作用,故选B,
故答案为:B.
| ||
| ||
故答案为:2Cl-+2H2O
| ||
②氯化铁做净水剂是因为Fe3+水为Fe(OH)3胶体的缘故,原理为Fe3++3H2O⇌Fe(OH)3(胶体)+3H+,
故答案为:Fe3++3H2O⇌Fe(OH)3(胶体)+3H+;
(2)吸收剂X的与Cl2反应的产物是FeCl3,X是FeCl2;Cl2与氢氧化钠反应生成NaClO和NaCl,其中NaClO能做氧化剂,所以Y为NaClO,
故答案为:FeCl2;NaClO;
(3)碱性条件下根据反应物和产物可知,反应①的离子方程式为3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O;
故答案为:3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O;
(4)25℃时Fe(OH)3的Ksp=4.0×10-38,反应Ⅱ后的溶液中c(Fe3+)=4.0×10-5mol/L,Ksp=c(Fe3+)×c3(OH-),c3(OH-)=
| 4.0×10-38 |
| 4.0×10-5 |
c(H+)=
| 10-14 |
| 10-11 |
故答案为:3;K2FeO4溶解度小,析出晶体,促进反应进行;
(5)洗涤剂的选择要求:要对K2FeO4水解能起到抑制作用的试剂,在选项中,A能让K2FeO4水解,B中稀KOH溶液显碱性,对K2FeO4水解能起到抑制作用,C和D中的铵根和三价铁离子易水解,且水解后显酸性,对K2FeO4水解能起到促进作用,故选B,
故答案为:B.
看了 氯化铁和高铁酸钾都是常见的水...的网友还看了以下:
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是[]以KCl和ZnCl2混合液为电 2020-03-30 …
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是()A.镀锌层破损后即对铁制品失 2020-04-25 …
下列说法中不正确的是A电磁继电器能解决用控制低压电路的通断间接控制高压电路的通断问题B通电螺线管又 2020-05-13 …
下列制备金属单质的方法或原理正确的是()A.在高温条件下,用H2还原MgO制备单质MgB.在通电条 2020-05-14 …
高压控制下为什么是晴天? 2020-06-25 …
电子感应加速器是利用感生电场使电子加速的设备.它的基本原理如图甲所示(上部分为俯视图,下部分为真空室 2020-11-01 …
右图是电子感应加速器的示意图,上、下为电磁铁的两个磁极,磁极之间有一今环形真空室,电子在真空室中做圆 2020-11-01 …
下列物质的用途或用法与其理由说明相一致的是()A.通常情况下输电电缆用铝制成,是因为铝是导电性最好的 2020-11-05 …
(2012•佛山)图为一电动拉门的部分控制电路和工作原理示意图,A为电动机,c为电磁铁,D为衔铁,E 2020-11-12 …
以下哪种说法是不完全正确的?A.控制母线电压为1.1倍额定电压时,灯泡电阻与附加电阻限定的电流应不大 2020-11-23 …