在重水D2O中存在电离:D2OD++OD-,因此,对D2O可以采用同pH一样的定义来规定pD,即pD=-lg[D+]。已知在某温度下,D2O达电离平衡时,[D+][OD-]=1.6×10-15mol2·L
在重水D 2 O中存在电离:D 2 O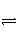
 D + +OD - ,因此,对D 2 O可以采用同pH一样的定义来规定pD,即pD=-lg[D + ]。已知在某温度下,D 2 O达电离平衡时,[D + ][OD - ]=1.6×10 -15 mol 2 ·L -2 ,则纯净的D 2 O在此温度下的pD________7(填“>”、“<”或“=”)。此温度下,若用0.01 mol DCl溶于D 2 O配成1 L溶液,pD________;若用0.01 mol NaOD溶于D 2 O配成1 L溶液时,pD________12(填“>”、“<”或“=”)。
D + +OD - ,因此,对D 2 O可以采用同pH一样的定义来规定pD,即pD=-lg[D + ]。已知在某温度下,D 2 O达电离平衡时,[D + ][OD - ]=1.6×10 -15 mol 2 ·L -2 ,则纯净的D 2 O在此温度下的pD________7(填“>”、“<”或“=”)。此温度下,若用0.01 mol DCl溶于D 2 O配成1 L溶液,pD________;若用0.01 mol NaOD溶于D 2 O配成1 L溶液时,pD________12(填“>”、“<”或“=”)。
已知:2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ·mol-1①2CH3OH(l 2020-04-07 …
已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH==CH3COO-+H+要使溶液中c( 2020-05-13 …
辅酶Ⅱ形成还原型辅酶Ⅱ的反应方程式为()A.NADP++2e-+H+NADPH+B.NADP++2 2020-05-15 …
醛固酮的主要作用是A.保Na+排K+B.保Na+保K+C.排Na+保K+D.排Na+排K+E.保H+ 2020-06-04 …
向含有Mn2+的酸性溶液中滴加过二硫酸钾(K2S2O8)溶液,会发生如下反应(未配平):Mn2++ 2020-07-02 …
△ABC中,∠ACB=90º,CD⊥AB于D,设AC=b,BC=a,AB=c,CD=h,求证(1) 2020-07-18 …
C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)C. 2020-07-24 …
25℃时,pH=4.75、浓度均为0.1mol·L-1的CH3COOH、CH3COONa混合溶液:为 2020-11-01 …
(2009年高考天津理综卷)下列说法正确的是()A.N+H→C+He是α衰变方程B.H+H→He+γ 2020-11-07 …
为什么求陡崖的相对高度要用(n-1)×d≦H<(n+1)×d其中d为等高距n表示重合的等高线条数?这 2020-11-19 …