早教吧作业答案频道 -->化学-->
电解原理在化学工业中有广泛应用.(1)电解食盐水是氯碱工业的基础.目前比较先进的方法是阳离子交换膜法,电解示意图如图1所示,图中的阳离子交换膜只允许阳离子通过,请回答以
题目详情
电解原理在化学工业中有广泛应用.
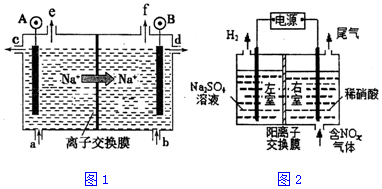
(1)电解食盐水是氯碱工业的基础.目前比较先进的方法是阳离子交换膜法,电解示意图如图1所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
①图中A极要连接电源的___(填“正”或“负”)极.
②精制饱和食盐水从图中___位置补充,氢氧化钠溶液从图中___位置流出.(选填“a”、“b”、“c”、“d”、“e”或“f”)
③电解总反应的离子方程式是___.
(2)电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图2所示(图中电极均为石墨电极).若用NO2气体进行模拟电解法吸收实验.
①写出电解时NO2发生反应的电极反应___.
②若有标准状况下2.24L NO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为___mol.
(3)为了减缓钢制品的腐蚀,可以在钢制品的表面镀铝.电解液采用一种非水体系的室温熔融盐,由有机阳离子、A12C17-和AlCl4-组成.
①钢制品应接电源的___极.
②己知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为___.
③若改用AlCl3水溶液作电解液,则阴极电极反应式为___.

(1)电解食盐水是氯碱工业的基础.目前比较先进的方法是阳离子交换膜法,电解示意图如图1所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
①图中A极要连接电源的___(填“正”或“负”)极.
②精制饱和食盐水从图中___位置补充,氢氧化钠溶液从图中___位置流出.(选填“a”、“b”、“c”、“d”、“e”或“f”)
③电解总反应的离子方程式是___.
(2)电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图2所示(图中电极均为石墨电极).若用NO2气体进行模拟电解法吸收实验.
①写出电解时NO2发生反应的电极反应___.
②若有标准状况下2.24L NO2被吸收,通过阳离子交换膜(只允许阳离子通过)的H+为___mol.
(3)为了减缓钢制品的腐蚀,可以在钢制品的表面镀铝.电解液采用一种非水体系的室温熔融盐,由有机阳离子、A12C17-和AlCl4-组成.
①钢制品应接电源的___极.
②己知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为___.
③若改用AlCl3水溶液作电解液,则阴极电极反应式为___.
▼优质解答
答案和解析
(1)①由电解食盐水装置图可知,钠离子移向右边,则左边A为阳极,所以A极要连接电源的正极,故答案为:正;
②由电解食盐水装置图可知,钠离子移向右边,则左边A为阳极,电极方程式为2Cl--2e-=Cl2↑,所以精制饱和食盐水从图中a位置补充,右边B为阴极,电极方程式为2H2O+2e-=H2↑+2OH- 或2H++2e-=H2↑,则生成氢氧化钠从图中d位置流出,
故答案为:a;d;
③电解总反应的离子方程式是2Cl-+2H2O
Cl2↑+H2↑+2OH-,
故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-;
(2)①根据图知,电解时,左室中电极上氢离子放电生成氢气,则左室为阴极室,右室为阳极室,阳极上通入的是氮氧化物,生成的硝酸,所以阳极上氮氧化物失电子和水生成硝酸,电极反应式为:NO2-e-+H2O=NO3-+2H+,
故答案为:NO2-e-+H2O=NO3-+2H+;
②n(NO2)=
=0.1mol,阳极反应式为NO2-e-+H2O=NO3-+2H+,有0.2mol氢离子生成,因为有0.1mol硝酸生成,则有0.1mol氢离子引入阴极室,
故答案为:0.1;
(3)①依据电镀原理分析,钢铁上镀铝是利用铝做阳极与电源正极相连,钢铁做阴极与电源负极相连,故答案为:负;
②由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体做电解液来实现,离子液体是一种室温熔融盐,为非水体系,电镀过程中不产生其他离子且有机阳离子不参与电极反应,则阴极反应生成铝是发生的还原反应,铝元素化合价降低,分析离子液体成分,结合电荷守恒分析可知是Al2Cl7-得到电子生成,电极反应为:4Al2Cl7-+3e-=Al+7AlCl4-;故答案为:4Al2Cl7-+3e-=Al+7AlCl4-;
③改用AlCl3水溶液作电解液是溶液中氢离子在阴极放电生成氢气,阴极反应式为2H++2e-=H2↑,故答案为:2H++2e-=H2↑.
②由电解食盐水装置图可知,钠离子移向右边,则左边A为阳极,电极方程式为2Cl--2e-=Cl2↑,所以精制饱和食盐水从图中a位置补充,右边B为阴极,电极方程式为2H2O+2e-=H2↑+2OH- 或2H++2e-=H2↑,则生成氢氧化钠从图中d位置流出,
故答案为:a;d;
③电解总反应的离子方程式是2Cl-+2H2O
| ||
故答案为:2Cl-+2H2O
| ||
(2)①根据图知,电解时,左室中电极上氢离子放电生成氢气,则左室为阴极室,右室为阳极室,阳极上通入的是氮氧化物,生成的硝酸,所以阳极上氮氧化物失电子和水生成硝酸,电极反应式为:NO2-e-+H2O=NO3-+2H+,
故答案为:NO2-e-+H2O=NO3-+2H+;
②n(NO2)=
| 2.24L |
| 22.4L/mol |
故答案为:0.1;
(3)①依据电镀原理分析,钢铁上镀铝是利用铝做阳极与电源正极相连,钢铁做阴极与电源负极相连,故答案为:负;
②由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体做电解液来实现,离子液体是一种室温熔融盐,为非水体系,电镀过程中不产生其他离子且有机阳离子不参与电极反应,则阴极反应生成铝是发生的还原反应,铝元素化合价降低,分析离子液体成分,结合电荷守恒分析可知是Al2Cl7-得到电子生成,电极反应为:4Al2Cl7-+3e-=Al+7AlCl4-;故答案为:4Al2Cl7-+3e-=Al+7AlCl4-;
③改用AlCl3水溶液作电解液是溶液中氢离子在阴极放电生成氢气,阴极反应式为2H++2e-=H2↑,故答案为:2H++2e-=H2↑.
看了电解原理在化学工业中有广泛应用...的网友还看了以下:
分子,原子,电子?万物是由许多许多的原素组成的,如何解释分子,原子的存在意义? 2020-05-12 …
铁元素不仅可以与SCN-、CN-等离子形成配合物,还可以与CO、NO等分子以及许多有机试剂形成配合 2020-05-13 …
铁元素不仅可以与SCN-、CN-等离子形成配合物,还可以与CO、NO等分子以及许多有机试剂形成配合 2020-05-13 …
下列关于金属的叙述中不正确的是A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间强烈的相互作 2020-05-15 …
一颗豆荚,里面有3粒豆子,请问它分别由几个子房,几个胚珠发育而来?每个西瓜里都有许多种子,是因为( 2020-06-28 …
一颗豆荚,里面有3粒豆子,请问它分别由几个子房,几个胚珠发育而来?每个西瓜里都有许多种子,是因为( 2020-06-28 …
“我这一辈子走过许多地方的路,行过许多地方的桥……”出自哪里?“我这一辈子走过许多地方的路,行过许 2020-07-07 …
某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内 2020-07-10 …
请高手翻译英文句子1.请尽快通过电子邮件与他们取得联系(getintouch)2.一旦你许下诺言, 2020-07-10 …
一种能快速充电的超常性能电池-铅离子电池.或许能更好的解决电网电力的存储、协调、平衡问题.该电池由A 2020-11-01 …