早教吧作业答案频道 -->化学-->
Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.Ⅰ.制备Na2S2O3•5H2O反应原理:Na2SO3(aq)+S(s)△.
题目详情
Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.
Ⅰ.制备Na2S2O3•5H2O 反应原理:Na2SO3(aq)+S(s)
Na2S2O3(aq)
实验步骤:
①称取15g Na2SO3加入圆底烧瓶中,再加入80ml蒸馏水.另取5g研细的硫粉,用3ml乙醇润湿,加入上述溶液中.
②安装实验装置(如图所示,部分加持装置略去),水浴加热,微沸60分钟.
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3•5H2O,经过滤,洗涤,干燥,得到产品.
回答问题:
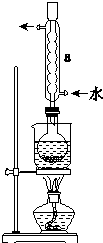
(1)仪器a的名称是___,其作用是___.
(2)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是___,检验是否存在该杂质的方法是___.
(3)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因:___.
Ⅱ.测定产品纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol•L‾1碘的标准溶液滴定,滴定至终点时,消耗标准溶液的体积为18.10mL.
反应原理为:2S2O32‾+I2═S4O62-+2I‾
(4)滴定至终点时,溶液颜色的变化:___.
(5)产品的纯度为(设Na2S2O3•5H2O相对分子质量为M)___.
Ⅲ.Na2S2O3的应用
(6)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42‾,常用作脱氧剂,该反应的离子方程式为___.
Ⅰ.制备Na2S2O3•5H2O 反应原理:Na2SO3(aq)+S(s)
| ||
实验步骤:
①称取15g Na2SO3加入圆底烧瓶中,再加入80ml蒸馏水.另取5g研细的硫粉,用3ml乙醇润湿,加入上述溶液中.
②安装实验装置(如图所示,部分加持装置略去),水浴加热,微沸60分钟.
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3•5H2O,经过滤,洗涤,干燥,得到产品.
回答问题:

(1)仪器a的名称是___,其作用是___.
(2)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是___,检验是否存在该杂质的方法是___.
(3)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因:___.
Ⅱ.测定产品纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol•L‾1碘的标准溶液滴定,滴定至终点时,消耗标准溶液的体积为18.10mL.
反应原理为:2S2O32‾+I2═S4O62-+2I‾
(4)滴定至终点时,溶液颜色的变化:___.
(5)产品的纯度为(设Na2S2O3•5H2O相对分子质量为M)___.
Ⅲ.Na2S2O3的应用
(6)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42‾,常用作脱氧剂,该反应的离子方程式为___.
▼优质解答
答案和解析
(1)根据图示中仪器的结构特征,可知仪器a为冷凝管,该实验中冷凝管具有冷凝回流的作用,
故答案为:冷凝管;冷凝回流;
(2)由于Na2S2O3、Na2SO3具有还原性,易被氧气氧化Na2SO4,所以可能存在的杂质是Na2SO4;检验硫酸钠的方法为:取少量产品溶于过量稀盐酸,过滤,向滤液中加BaCl2溶液,若有白色沉淀,则产品中含有Na2SO4,
故答案为:Na2SO4; 取少量产品溶于过量稀盐酸,过滤,向滤液中加BaCl2溶液,若有白色沉淀,则产品中含有Na2SO4;
(3)S2O32‾与氢离子发生氧化还原反应生成淡黄色硫单质,反应的离子方程式为:S2O32‾+2H+=S↓+SO2↑+H2O,
故答案为:S2O32‾+2H+=S↓+SO2↑+H2O;
(4)滴定结束后,碘单质使淀粉变蓝,所以滴定终点时溶液颜色变化为:由无色变为蓝色,
故答案为:由无色变为蓝色;
(5)根据反应2S2O32-+I2═S4O62-+2I-可知,n(S2O32-)=2n(I2),所以W g产品中含有Na2S2O3•5H2O质量为:0.1000 mol•L-1×18.10×10-3L×2×M=3.620×10-3Mg,则产品的纯度为:
×100%=
×100%,
故答案为:
×100%;
(6)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,根据化合价升降相等配平后的离子方程式为:S2O32‾+4Cl2+5H2O=2SO42‾+8Cl‾+10H+,
故答案为:S2O32‾+4Cl2+5H2O=2SO42‾+8Cl‾+10H+.
故答案为:冷凝管;冷凝回流;
(2)由于Na2S2O3、Na2SO3具有还原性,易被氧气氧化Na2SO4,所以可能存在的杂质是Na2SO4;检验硫酸钠的方法为:取少量产品溶于过量稀盐酸,过滤,向滤液中加BaCl2溶液,若有白色沉淀,则产品中含有Na2SO4,
故答案为:Na2SO4; 取少量产品溶于过量稀盐酸,过滤,向滤液中加BaCl2溶液,若有白色沉淀,则产品中含有Na2SO4;
(3)S2O32‾与氢离子发生氧化还原反应生成淡黄色硫单质,反应的离子方程式为:S2O32‾+2H+=S↓+SO2↑+H2O,
故答案为:S2O32‾+2H+=S↓+SO2↑+H2O;
(4)滴定结束后,碘单质使淀粉变蓝,所以滴定终点时溶液颜色变化为:由无色变为蓝色,
故答案为:由无色变为蓝色;
(5)根据反应2S2O32-+I2═S4O62-+2I-可知,n(S2O32-)=2n(I2),所以W g产品中含有Na2S2O3•5H2O质量为:0.1000 mol•L-1×18.10×10-3L×2×M=3.620×10-3Mg,则产品的纯度为:
| 3.620×10-3Mg |
| Wg |
| 3.620×10-3Mg |
| Wg |
故答案为:
| 3.620×10-3Mg |
| Wg |
(6)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,根据化合价升降相等配平后的离子方程式为:S2O32‾+4Cl2+5H2O=2SO42‾+8Cl‾+10H+,
故答案为:S2O32‾+4Cl2+5H2O=2SO42‾+8Cl‾+10H+.
看了Na2S2O3是重要的化工原料...的网友还看了以下:
设NA为阿佛加德罗常数(1)4.9g硫酸中含有molH原子,个O原子和个S原子,与克H2O中所含O 2020-04-13 …
为什么硫酸根带两个单位的负电荷呢?S的化合价是+6,O的化合价是-2.那么S丢失的6个电子在哪?若 2020-05-13 …
1质量相等的SO2和SO3(1)所含S元素的质量比(2)S原子的个数比2在FeOFe2O3Fe3O 2020-06-06 …
点A、B、O分别以5个单位/s,2单位/s,1单位/s的速度向右移运动,几秒后,o点恰好成为线段中 2020-06-15 …
0.05mol硫酸含有 molH原子,molS原子,molO原子,含有 个H原子,个S原子,个O原 2020-06-27 …
直线l:y=mx+1与椭圆c:ax^2+y^2=2交于A、B;两点,以OA、OB为邻边做平行四边形 2020-07-24 …
如图,DE是⊙O的直径,CE与⊙O相切,E为切点.连接CD交⊙O于点B,在EC上取一个点F,使EF 2020-07-31 …
金属元素Al、Co、Cu可与C、H、N、O、S等形成多种化合物.(1)C、N、O、S四种元素的第一电 2020-11-03 …
已知直线L:Y=K(x+2根号2)与圆O:x平方+y平方=4相交于A、B两点,O是坐标原点,三角形A 2021-01-11 …
1.查阅有关资料,列举几个实例,说明分类法对于化学科学发展的重要意义.2.O、S、H、Ca组成的物质 2021-01-23 …