早教吧作业答案频道 -->化学-->
亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌.以下是制取亚氯酸钠的工艺流程:已知:ClO2气体在中性和碱性溶液中不能稳定存在,且只能保持在浓度
题目详情
亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌.以下是制 取亚氯酸钠的工艺流程:
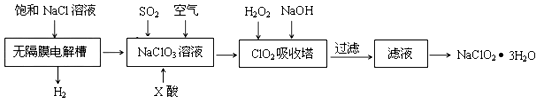
已知:ClO2气体在中性和碱性溶液中不能稳定存在,且只能保持在浓度较低状态下以防止爆炸性分解,需现合成现用.
(1)在无隔膜电解槽中持续电解一段时间后,生成氢气和NaClO3,请写出阳极的电极反应方程式:___.
(2)反应生成ClO2气体需要X酸酸化,X酸可以为___.
A.稀硫酸 B.盐酸 C.硝酸 D.H2C2O4溶液
(3)ClO2吸收塔内的温度不能过高,其原因为:___
(4)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果.某工厂污水中含CN-amg/L,现用ClO2和CN-氧化,生成了两种无毒无害的气体,其离子反应方程式为___;处理100m3这种污水,反应过程转移的电子数为___.

已知:ClO2气体在中性和碱性溶液中不能稳定存在,且只能保持在浓度较低状态下以防止爆炸性分解,需现合成现用.
(1)在无隔膜电解槽中持续电解一段时间后,生成氢气和NaClO3,请写出阳极的电极反应方程式:___.
(2)反应生成ClO2气体需要X酸酸化,X酸可以为___.
A.稀硫酸 B.盐酸 C.硝酸 D.H2C2O4溶液
(3)ClO2吸收塔内的温度不能过高,其原因为:___
(4)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果.某工厂污水中含CN-amg/L,现用ClO2和CN-氧化,生成了两种无毒无害的气体,其离子反应方程式为___;处理100m3这种污水,反应过程转移的电子数为___.
▼优质解答
答案和解析
(1)电解池中阳极失去电子,所以溶液中的氯离子在阳极失去电子,生成氢气和NaClO3,因此反应的电极反应式是Cl--6e-+6OH-=ClO3-+3H2O;
故答案为:Cl--6e-+6OH-=ClO3-+3H2O;
(2)由于ClO2气体在中性和碱性溶液中不能稳定存在,所以只能在酸性环境中存在,由于在酸性条件下,氯酸钠容易和盐酸、硝酸、草酸发生氧化还原反应,所以X应该是硫酸;
故答案为:A;
(3)H2O2不稳定,温度过高,H2O2容易分解,吸收塔的温度不能过高,其目的是防止H2O2分解;
故答案为:温度过高H2O2将分解;
(4)ClO2将CN-氧化,生成了两种无毒无害的气体即二氧化碳和氮气,所以离子方程式为:2ClO2+2CN-=2Cl-+2CO2+N2↑;该反应2molCN-转移10mol电子,根据方程式1molCN-离子消耗1mol二氧化氯,所以处理100m3这种污水,含有的CN-为
=
mol,则转移电子数:
×
NA=
NA;
故答案为:2ClO2+2CN-=2Cl-+2CO2+N2↑;
NA.
故答案为:Cl--6e-+6OH-=ClO3-+3H2O;
(2)由于ClO2气体在中性和碱性溶液中不能稳定存在,所以只能在酸性环境中存在,由于在酸性条件下,氯酸钠容易和盐酸、硝酸、草酸发生氧化还原反应,所以X应该是硫酸;
故答案为:A;
(3)H2O2不稳定,温度过高,H2O2容易分解,吸收塔的温度不能过高,其目的是防止H2O2分解;
故答案为:温度过高H2O2将分解;
(4)ClO2将CN-氧化,生成了两种无毒无害的气体即二氧化碳和氮气,所以离子方程式为:2ClO2+2CN-=2Cl-+2CO2+N2↑;该反应2molCN-转移10mol电子,根据方程式1molCN-离子消耗1mol二氧化氯,所以处理100m3这种污水,含有的CN-为
| 100×103mL×a×10-3mg/L |
| 26g/mol |
| 100a |
| 26 |
| 100a |
| 26 |
| 10 |
| 2 |
| 250a |
| 13 |
故答案为:2ClO2+2CN-=2Cl-+2CO2+N2↑;
| 250a |
| 13 |
看了亚氯酸钠(NaClO2)是一种...的网友还看了以下:
当物体沿半圆轨道下滑,下滑过程中是超重还是失重,如何判断我们只能确定支持力比重力在支持力反方向上的 2020-04-26 …
在科学实践课上,王老师将一只模型鸟的尖嘴支在矿泉水瓶盖上,模型鸟的整个身体就能悬空保持平衡,如图所 2020-06-17 …
如图所示,一人推着重物在水平路面上匀速向前运动的过程中,重物受到重力、推力、滑动摩擦力和支持力的作 2020-06-25 …
1.农妇对妻子说:“如果卖掉75只小鸡,那么咱们的饲料还能维持20天,然而照你的建议,在买进100 2020-07-10 …
阅读下面的文字,根据要求作文。秋天,葡萄熟了,高高的葡萄架下来了一只只馋嘴的狐狸。第一只狐狸在葡萄架 2020-11-03 …
motoGP中车手过弯压车问题motoGP中车手过弯需要压车,但从力学角度来看,车与人只受重力,支持 2020-11-26 …
举重运动员在地上能举起120kg的重物,在竖直向上举重运动员在地上能举起120kg的重物,在竖直方向 2020-11-26 …
这道题怎么做:我们参与社会生活所必我们参与社会生活所必须遵守的重要原则是[]A.依法治国与以德治国并 2020-11-28 …
从1949年苏联第一次在联合国要求恢复新中国的合法席位到1971年的20多年间,苏联对新中国重返联合 2020-12-05 …
嗨,迈克①迈克得了一种罕见的病.他的脖子僵直,身体僵硬,肌肉一点一点地萎缩.他的病情越来越重,最后完 2021-01-16 …