早教吧作业答案频道 -->化学-->
高纯度的氢氧化镁广泛应用于医药、电力等领域.镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如下:己知1:溶液I中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子2:几种金属阳离子的氢
题目详情
高纯度的氢氧化镁广泛应用于医药、电力等领域.镁硅酸盐矿石可用于生产氢氧化镁,简要工艺流程如下:
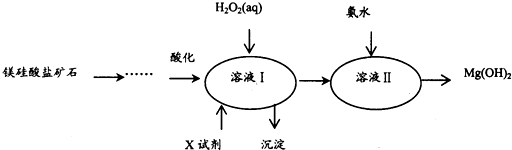
己知1:溶液I中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子
2:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
(1)Mg在周期表中的位置___,Si的原子结构示意图为___.
(2)向溶液I中加入X的作用是___.
(3)向溶液I中加入的两种试剂先后顺序是___(填化学式).
(4)加入H2O2溶液反应的离子方程式是___.
(5)如图是溶液Ⅱ中Mg2+转化率随温度t的变化示意图:
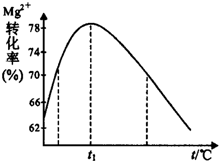
①向溶液Ⅱ中加入氨水反应的离子方程式是___.
②t1前Mg2+转化率增大的原因是___;t1后Mg2+转化率下降的原因是(用化学方程式表示)___.

己知1:溶液I中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子
2:几种金属阳离子的氢氧化物沉淀时的pH如下表所示:
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
(2)向溶液I中加入X的作用是___.
(3)向溶液I中加入的两种试剂先后顺序是___(填化学式).
(4)加入H2O2溶液反应的离子方程式是___.
(5)如图是溶液Ⅱ中Mg2+转化率随温度t的变化示意图:

①向溶液Ⅱ中加入氨水反应的离子方程式是___.
②t1前Mg2+转化率增大的原因是___;t1后Mg2+转化率下降的原因是(用化学方程式表示)___.
▼优质解答
答案和解析
溶液Ⅰ中除MgSO4外,还含有少量Fe3+、Al3+、Fe2+等离子,根据题中提供的各种金属离子沉淀的pH值可知,加入双氧水可以将亚铁离子氧化成铁离子,再加入试剂X主要作用是调节溶液pH值,使铁离子沉淀,可以加氧化镁或氢氧化镁等,过滤后在滤液中加入氨水使溶液中镁离子沉淀,得氢氧化镁沉淀,由于要通过使铁离子沉淀的方法除去铁,所以要先氧化再沉淀,根据Mg2+转化率随温度t的变化示意图可知,由于氨水与镁离子反应生成氢氧化镁的反应是吸热反应,所以升高温度,镁离子的转化率增大,但随着温度的升高,氨气在水中的溶解度减小,氨水的浓度减小,会导致Mg2+转化率减小,
(1)Mg的原子序数为12,原子核外有3个电子层,最外层电子数为2,则位于周期表第三周期ⅡA族,Si的原子核外有3个电子层,最外层电子数为4,原子结构示意图为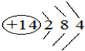 ,
,
故答案为:第三周期ⅡA族;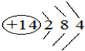 ;
;
(2)根据上面的分析可知,向溶液Ⅰ中加入X的作用是调节溶液pH,
故答案为:调节溶液pH;
(3)根据上面的分析可知,要先氧化再沉淀,所以向溶液Ⅰ中加入的两种试剂先后顺序是H2O2、MgO[Mg(OH)2或MgCO3],故答案为:H2O2、MgO[Mg(OH)2或MgCO3];
(4)根据上面的分析可知,加入H2O2溶液反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(5)①向溶液Ⅱ中加入氨水与镁离子反应生成氢氧化镁沉淀,反应的离子方程式是 Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+,
故答案为:Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+;
②根据上面的分析可知,t1前Mg2+转化率增大的原因是 升高温度,Mg2+转化率增大,平衡右移,反应是吸热反应;t1后Mg2+转化率下降的原因是氨气在水中的溶解度减小,氨水的浓度减小,反应的方程式为 NH3•H2O
NH3↑+H2O,
故答案为:镁离子与氨水反应是吸热反应,升高温度,平衡右移,Mg2+转化率增大;NH3•H2O
NH3↑+H2O.
(1)Mg的原子序数为12,原子核外有3个电子层,最外层电子数为2,则位于周期表第三周期ⅡA族,Si的原子核外有3个电子层,最外层电子数为4,原子结构示意图为
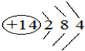 ,
,故答案为:第三周期ⅡA族;
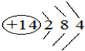 ;
;(2)根据上面的分析可知,向溶液Ⅰ中加入X的作用是调节溶液pH,
故答案为:调节溶液pH;
(3)根据上面的分析可知,要先氧化再沉淀,所以向溶液Ⅰ中加入的两种试剂先后顺序是H2O2、MgO[Mg(OH)2或MgCO3],故答案为:H2O2、MgO[Mg(OH)2或MgCO3];
(4)根据上面的分析可知,加入H2O2溶液反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(5)①向溶液Ⅱ中加入氨水与镁离子反应生成氢氧化镁沉淀,反应的离子方程式是 Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+,
故答案为:Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+;
②根据上面的分析可知,t1前Mg2+转化率增大的原因是 升高温度,Mg2+转化率增大,平衡右移,反应是吸热反应;t1后Mg2+转化率下降的原因是氨气在水中的溶解度减小,氨水的浓度减小,反应的方程式为 NH3•H2O
| ||
故答案为:镁离子与氨水反应是吸热反应,升高温度,平衡右移,Mg2+转化率增大;NH3•H2O
| ||
看了高纯度的氢氧化镁广泛应用于医药...的网友还看了以下:
求解一道数学题用一元二次方程解一容器盛满纯药液20升,第一次倒出若干升后用水加满;第二次又倒出同等 2020-05-16 …
铵盐都是白色晶体1铵盐纯度较高2铵盐都晶体吗?3铵盐白色的吗,有没有无色的,或黄色的4铵盐加热都生 2020-05-17 …
外加涉及到的公式~一个容器盛满20L纯药液,倒出一部分后,用水加满,第二次又倒出同样多的液体,再用 2020-06-27 …
一个容器盛满纯药液63L,第一次倒出一部分纯药液后,用水加满,第二次又倒出同样多的药液,这时容器内 2020-06-30 …
(2008•茂名二模)如果误食亚硝酸盐会使人中毒,因为亚硝酸盐会使Fe2+转变为Fe3+生成高铁血红 2020-11-12 …
初3数学题``关于一元2次方程的运用~!``一个容器盛满纯药63L,第一次倒出一部分药液后加满水,第 2020-11-17 …
初三数学一个容器盛满纯药液63升,第一次倒出一部分后,用水加满,第二次倒出同样多的药液,再用水加满, 2020-11-24 …
人体血红蛋白中含有Fe2+,如果误食亚硝酸盐会使人体中毒,因为亚硝酸盐能使Fe2+转化为Fe3+,生 2020-12-03 …
一种喷洒果树的药水,纯药液和水的比是1:200,要配置这种药水60.3千克,需纯药液克. 2020-12-22 …
一种喷洒果树的药水,其纯药液和水质量比是1:50,现配置这种药水45.3kg,需纯药液g. 2020-12-22 …