早教吧作业答案频道 -->化学-->
探究SO2的性质.甲组同学将SO2分别通入下列3种溶液中.SO2气体KMnO4酸性溶液品红溶液NaOH和BaCl2的混合溶液(1)试管a中观察到的现象是.(2)试管b中观察到紫色褪去,说明SO2具有的性质
题目详情
探究SO2的性质.甲组同学将SO2分别通入下列3种溶液中.
SO2气体KMnO4酸性溶液品红溶液NaOH和BaCl2的混合溶液
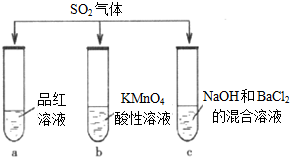
(1)试管a中观察到的现象是___.
(2)试管b中观察到紫色褪去,说明SO2具有的性质是___.
(3)试管c中产生了能溶于稀盐酸的白色沉淀,该白色沉淀是___.
(4)乙组同学多做了一组实验,他们将SO2通入盛有1.0mol/L Fe(NO3)3和BaCl2的混合溶液(已知1.0mol/L Fe(NO3)3溶液中c(H+)=0.1mol/L)的试管d中,得到了不溶于稀盐酸的白色沉淀.分析产生该白色沉淀的原因:
观点1:SO2与Fe3+反应
观点2:在酸性条件下SO2与NO3-反应
观点3:___.
欲证明观点2,只需将试管d中Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验.应选择的试剂是___(填字母).
a.0.1mol/L稀硝酸
b.1.5mol/L Ba(NO3)2和0.1mol/L HNO3的混合溶液
c.6.0mol/L NaNO3和0.2mol/L盐酸等体积混合的溶液.
SO2气体KMnO4酸性溶液品红溶液NaOH和BaCl2的混合溶液

(1)试管a中观察到的现象是___.
(2)试管b中观察到紫色褪去,说明SO2具有的性质是___.
(3)试管c中产生了能溶于稀盐酸的白色沉淀,该白色沉淀是___.
(4)乙组同学多做了一组实验,他们将SO2通入盛有1.0mol/L Fe(NO3)3和BaCl2的混合溶液(已知1.0mol/L Fe(NO3)3溶液中c(H+)=0.1mol/L)的试管d中,得到了不溶于稀盐酸的白色沉淀.分析产生该白色沉淀的原因:
观点1:SO2与Fe3+反应
观点2:在酸性条件下SO2与NO3-反应
观点3:___.
欲证明观点2,只需将试管d中Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验.应选择的试剂是___(填字母).
a.0.1mol/L稀硝酸
b.1.5mol/L Ba(NO3)2和0.1mol/L HNO3的混合溶液
c.6.0mol/L NaNO3和0.2mol/L盐酸等体积混合的溶液.
▼优质解答
答案和解析
(1)二氧化硫具有漂白性,能够使品红溶液褪色,故答案为:溶液褪色;
(2)二氧化硫具有还原性能够还原酸性的高锰酸钾,使高锰酸钾褪色,故答案为:还原性;
(3)二氧化硫为酸性氧化物,能够与氢氧化钠反应生成亚硫酸钠,亚硫酸钠与氯化钡反应生成亚硫酸钡沉淀,亚硫酸钡与盐酸反应生成氯化钡和二氧化硫和水;
故答案为:BaSO3;
(4)Fe3+、酸性条件下NO3-都能氧化SO2,即SO2和Fe3+、酸性条件下的NO3-都反应,所以可能情况有三种:
观点1:SO2与Fe3+反应,
观点2:在酸性条件下SO2与NO3-反应,
观点3:SO2和Fe3+、酸性条件下NO3-都反应;
要证明观点2:在酸性条件下SO2与NO3-反应,则需要排除三价铁离子的干扰,选择酸性环境下的硝酸根离子,只有c合理,
故答案为:SO2和Fe3+、酸性条件下NO3-都反应;c.
(2)二氧化硫具有还原性能够还原酸性的高锰酸钾,使高锰酸钾褪色,故答案为:还原性;
(3)二氧化硫为酸性氧化物,能够与氢氧化钠反应生成亚硫酸钠,亚硫酸钠与氯化钡反应生成亚硫酸钡沉淀,亚硫酸钡与盐酸反应生成氯化钡和二氧化硫和水;
故答案为:BaSO3;
(4)Fe3+、酸性条件下NO3-都能氧化SO2,即SO2和Fe3+、酸性条件下的NO3-都反应,所以可能情况有三种:
观点1:SO2与Fe3+反应,
观点2:在酸性条件下SO2与NO3-反应,
观点3:SO2和Fe3+、酸性条件下NO3-都反应;
要证明观点2:在酸性条件下SO2与NO3-反应,则需要排除三价铁离子的干扰,选择酸性环境下的硝酸根离子,只有c合理,
故答案为:SO2和Fe3+、酸性条件下NO3-都反应;c.
看了探究SO2的性质.甲组同学将S...的网友还看了以下:
1.课外小组的女同学原来占全组人数的三分之一,加入4名女同学后,恰好占全组人数的一半,则课外小组原 2020-04-26 …
中考化学计算题.求详解某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0g石灰石样品 2020-04-27 …
根据描述,在空格中填上与其相对应的化学用语:(1)最清洁的气体燃料(填化学式);(2)食品袋内常充 2020-05-02 …
有关化学的知识!急!1.人体中含钙量最多的是A.肌肉.B.骨骼.C.韧带D.血液2.食品污染是指A 2020-05-13 …
某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0 g石灰石样品,把25.0g质量分 2020-05-13 …
某学生用一架不等臂天平称药品,第一次将左盘放入50克砝码,右盘子放入药品使天平平衡,第二次将右盘放 2020-07-04 …
一道java入门的题求解题目为:一家公司销售物种不同的商品,零售价为:商品1.$2.98,商品2. 2020-07-17 …
(10分)某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0g石灰石样品,把25.0 2020-07-26 …
生活中处处有化学,家庭厨房就是一个化学小世界.(1)充入食品包装袋中可防腐的单质(填化学式,下同); 2020-12-10 …
经济学预算线:商品1的数量为30,商品二的数量为20,商品二的价格为2,曲线I为消费者无差异曲线,I 2020-12-23 …