已知:H2SO3⇌HSO-3+H+Ka1、HSO-3⇌SO2-3+H+Ka2常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-和SO32-三种微粒的物质的量分数与溶液的关系如图所
已知:H2SO3⇌HSO
+H+ Ka1、HSO
⇌SO
+H+ Ka2
常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-和SO32-三种微粒的物质的量分数与溶液的关系如图所示,则下列说法中不正确的是( )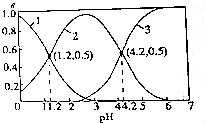
A. 曲线3表示的微粒是SO32-
B. 溶液pH=4.2时,c(Na+)+c(H+)=c(OH-)+2c(SO32-)
C. 常温下,
=1000Ka1 Ka2
D. 溶液pH=1.2时:c(Na+)+c(H+)=c(OH-)+c(HSO3)
B.溶液pH=4.2时,根据电荷守恒可知:c(Na+)+c(H+)=c(OH-)+2c(SO32-)+c(HSO3-),故B错误;
C.坐标(1.2,0.5)时H2SO3、HSO3-的含量相同,则Ka1=c(H+)=10-1.2,坐标(4.2,0.5)时HSO3-和SO32-的浓度相等,Ka2=c(H+)=10-4.2,则
| Ka1 |
| Ka2 |
| 10-1.2 |
| 10-4.2 |
D.溶液pH=1.2时每公斤电荷守恒可知:c(Na+)+c(H+)=c(OH-)+c(HSO3),故D正确;
故选B.
1.发生结晶现象的溶液().A.一定是浓溶液B.一定是稀溶液.C.一定是饱和溶液.D.可能是饱和溶 2020-04-12 …
在ph=2的条件下,将含有高锰酸根,铁离子,亚铁离子和碘离子的四种溶液混合充分反应后1.溶液中有碘 2020-05-14 …
在一定体积c(OH-)=0.01mol/L的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaH 2020-05-14 …
1.配置一定物质的量溶度溶液时,容量瓶水洗后可不干燥对吗?2.液态的醋酸是电解质吗?3.用氯化铵浓 2020-06-06 …
如图是实验室配制一定溶质质量分数的NaCl溶液的流程图.请回答:(1)应称量gNaCl,需加水mL 2020-06-27 …
(2008•宿州二模)玻璃棒是中学化学常用仪器,在下列实验中,都用到玻璃棒:①粗盐提纯②一定溶质的质 2020-11-12 …
常温条件下,将SO2气体通入一定量NaOH溶液中,所得溶液呈中性,关于该溶液的判断错误的是()A.该 2020-11-27 …
实验室常用来测定溶液的酸碱性.实验室最常用来测定溶液的酸碱度.pH试纸测溶液pH的正确操作方法.用p 2020-12-02 …
溶液的酸碱度测定:溶液的酸碱度可以用pH试纸pH试纸来测定,用pHpH表示,当pH=0时溶液呈酸酸性 2020-12-02 …
为测定某H2C2O4溶液的浓度,取该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为cmol/LKM 2020-12-25 …