早教吧作业答案频道 -->化学-->
碱式次氯酸镁[BMH化学式为Mg2ClO(OH)3•H2O]难溶于水,相对稳定,是一种有开发价值的无机抗菌剂.某研发小组通过下列流程制备碱式次氯酸镁:(1)在上述流程中,“过滤”操作用到的硅
题目详情
碱式次氯酸镁[BMH化学式为Mg2ClO(OH)3•H2O]难溶于水,相对稳定,是一种有开发价值的无机抗菌剂.某研发小组通过下列流程制备碱式次氯酸镁:
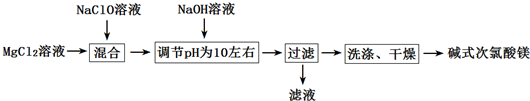
(1)在上述流程中,“过滤”操作用到的硅酸盐材质的仪器有___
(2)NaClO的电子式为___,NaClO溶液可用Cl2与NaOH溶液反应获得,写出该反应的离子方程式___
(3)有效氯的含量是衡量次氯酸盐氧化能力的重要指标.次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量来表示,则生成氯气的离子方程式为___
(4)就抗菌和杀菌效果而言,氯制剂具有广谱、高效的特点,像BMH这样难溶又稳定的氯制剂几乎别无他物.在酸性溶液中BMH具有杀菌、漂白作用的原因是___(用离子方程式表示)
(5)在混合溶液中加入NaOH溶液并调节pH在10左右,即生成BMH,其化学方程式为___.232

2

(1)在上述流程中,“过滤”操作用到的硅酸盐材质的仪器有___
(2)NaClO的电子式为___,NaClO溶液可用Cl2与NaOH溶液反应获得,写出该反应的离子方程式___
(3)有效氯的含量是衡量次氯酸盐氧化能力的重要指标.次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量来表示,则生成氯气的离子方程式为___
(4)就抗菌和杀菌效果而言,氯制剂具有广谱、高效的特点,像BMH这样难溶又稳定的氯制剂几乎别无他物.在酸性溶液中BMH具有杀菌、漂白作用的原因是___(用离子方程式表示)
(5)在混合溶液中加入NaOH溶液并调节pH在10左右,即生成BMH,其化学方程式为___.232

2
▼优质解答
答案和解析
氯化镁溶液与次氯酸钠溶液混合后,加入氢氧化钠溶液调节溶液pH,发生反应:2MgCl22+NaClO+3NaOH+H22O=Mg22ClO(OH)33•H22O↓+4NaCl,然后通过通过过滤、洗涤、干燥获得碱式次氯酸镁,
(1)过滤操作时需要用到的硅酸盐仪器有玻璃棒、烧杯、漏斗,
故答案为:烧杯、玻璃棒、漏斗;
(2)NaClO是离子化合物,由Na++离子和ClO--离子构成,NaClO的电子式为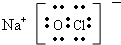 ;氯气与氢氧化钠溶液反应的离子方程式为:Cl22+2OH--=Cl--+ClO--+H22O,
;氯气与氢氧化钠溶液反应的离子方程式为:Cl22+2OH--=Cl--+ClO--+H22O,
故答案为: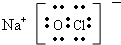 ;Cl22+2OH--=Cl--+ClO--+H22O;
;Cl22+2OH--=Cl--+ClO--+H22O;
(3)次氯酸盐与盐酸反应所生成的氯气,反应的离子方程式为:Cl--+ClO--+2H++=Cl22↑+H22O,
故答案为:Cl--+ClO--+2H++=Cl22↑+H22O;
(4)Mg22ClO(OH)33•H22O在酸性条件下发生反应:Mg22ClO(OH)33•H22O+4H++=2Mg2+2++HClO+4H22O,反应生成的次氯酸具有强氧化性,所以在酸性溶液中BMH具有杀菌、漂白作用,
故答案为:Mg22ClO(OH)33•H22O+4H++=2Mg2+2++HClO+4H22O;
(5)在混合溶液中加入NaOH溶液并调节pH在10左右,即生成BMH,反应的化学方程式为:2MgCl22+NaClO+3NaOH+H22O=Mg22ClO(OH)33•H22O↓+4NaCl,
故答案为:2MgCl22+NaClO+3NaOH+H22O=Mg22ClO(OH)33•H22O↓+4NaCl.
(1)过滤操作时需要用到的硅酸盐仪器有玻璃棒、烧杯、漏斗,
故答案为:烧杯、玻璃棒、漏斗;
(2)NaClO是离子化合物,由Na++离子和ClO--离子构成,NaClO的电子式为
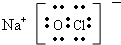 ;氯气与氢氧化钠溶液反应的离子方程式为:Cl22+2OH--=Cl--+ClO--+H22O,
;氯气与氢氧化钠溶液反应的离子方程式为:Cl22+2OH--=Cl--+ClO--+H22O,故答案为:
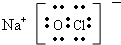 ;Cl22+2OH--=Cl--+ClO--+H22O;
;Cl22+2OH--=Cl--+ClO--+H22O;(3)次氯酸盐与盐酸反应所生成的氯气,反应的离子方程式为:Cl--+ClO--+2H++=Cl22↑+H22O,
故答案为:Cl--+ClO--+2H++=Cl22↑+H22O;
(4)Mg22ClO(OH)33•H22O在酸性条件下发生反应:Mg22ClO(OH)33•H22O+4H++=2Mg2+2++HClO+4H22O,反应生成的次氯酸具有强氧化性,所以在酸性溶液中BMH具有杀菌、漂白作用,
故答案为:Mg22ClO(OH)33•H22O+4H++=2Mg2+2++HClO+4H22O;
(5)在混合溶液中加入NaOH溶液并调节pH在10左右,即生成BMH,反应的化学方程式为:2MgCl22+NaClO+3NaOH+H22O=Mg22ClO(OH)33•H22O↓+4NaCl,
故答案为:2MgCl22+NaClO+3NaOH+H22O=Mg22ClO(OH)33•H22O↓+4NaCl.
看了 碱式次氯酸镁[BMH化学式为...的网友还看了以下:
已知代数式x的平方-5x+7,用配方法说明:不论x取何值,这个代数式的值总是正数.当x取何值时,这 2020-05-13 …
①②③因式分解,④⑤填空,⑥应用①6(x+y)^3-24(x+y)②x^2-x-2③a-b+ax- 2020-05-13 …
求|x-3|+|x+1|的最小值问下、是求x的最小值还是求算式的最小值?还有一题哝。|x-1|+| 2020-05-13 …
如何小概率事件?计算小概率事件的凯利公式是什么?有知道凯利计算公式的吗?听说该公式极其复杂,实际的 2020-05-16 …
1.已知x²+X-1=0,求x³+2x²+3的值 42.无论xy取何值,代数式x²+y²+2x-4 2020-05-17 …
一天,小明在纸上写了一个算式:4x2+8x+11,并对小刚说:“无论x取何值,这个代数式的值都是正 2020-06-21 …
用配方法说明,无论x取何值,代数式x的平方–6x+10的值用大于0,再求当x取何值时,代数式x的平 2020-06-24 …
式子|m-3|+6的值随m的变化而变化,当m=时,|m-3|+6有最小值,最小值是式子|m-3|+ 2020-06-30 …
已知代数式x2-5x+7,先用配方法说明,不论x取何值,这个代数式的值总是正数;再求出当x取何值时 2020-07-13 …
若0小于X小于1,则x(3-x)取最大值时X等于多少?大姐x取值在01中间哪有3啊是2次不等式是小 2020-07-21 …