早教吧作业答案频道 -->化学-->
废旧显示屏玻璃中含SiO2、Fe2O3、CeO2、FeO等物质.某课题小组以此玻璃粉末为原料,制得Ce(OH)4和硫酸铁铵矾[Fe2(SO4)3•(NH4)2SO4•24H2O],流程设计如下:已知:Ⅰ.酸性条件下,铈在
题目详情
废旧显示屏玻璃中含SiO2、Fe2O3、CeO2、FeO等物质.某课题小组以此玻璃粉末为原料,制得Ce(OH)4和硫酸铁铵矾[Fe2(SO4) 3•(NH4) 2SO4•24H2O],流程设计如下:
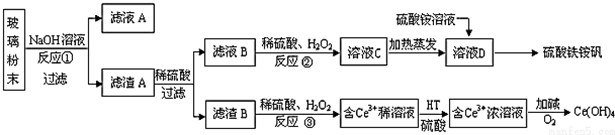
已知:Ⅰ.酸性条件下,铈在水溶液中有Ce3+、Ce4+两种主要存在形式,Ce4+有较强氧化性;
Ⅱ.CeO2不溶于稀硫酸,也不溶于NaOH溶液.回答以下问题:
(1)反应①的离子方程式是___.
(2)反应②中H2O2的作用是___.
(3)反应③的离子方程式是___.
(4)已知有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为:2Ce3+(水层)+6HT(有机层)⇌2CeT3 (有机层)+6H+(水层)
从平衡角度解释:向CeT3 (有机层)加入H2SO4 获得较纯的含Ce3+的水溶液的原因是___.
(5)硫酸铁铵矾[Fe2(SO4) 3•(NH4) 2SO4•24H2O]广泛用于水的净化处理,其净水原理用离子方程式解释是___.
(6)相同物质的量浓度的以下三种溶液中,NH4+的浓度由大到小的顺序是___.
a.Fe2(SO4) 3•(NH4) 2SO4•24H2O b.(NH4) 2SO4 c.(NH4) 2CO3.

已知:Ⅰ.酸性条件下,铈在水溶液中有Ce3+、Ce4+两种主要存在形式,Ce4+有较强氧化性;
Ⅱ.CeO2不溶于稀硫酸,也不溶于NaOH溶液.回答以下问题:
(1)反应①的离子方程式是___.
(2)反应②中H2O2的作用是___.
(3)反应③的离子方程式是___.
(4)已知有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为:2Ce3+(水层)+6HT(有机层)⇌2CeT3 (有机层)+6H+(水层)
从平衡角度解释:向CeT3 (有机层)加入H2SO4 获得较纯的含Ce3+的水溶液的原因是___.
(5)硫酸铁铵矾[Fe2(SO4) 3•(NH4) 2SO4•24H2O]广泛用于水的净化处理,其净水原理用离子方程式解释是___.
(6)相同物质的量浓度的以下三种溶液中,NH4+的浓度由大到小的顺序是___.
a.Fe2(SO4) 3•(NH4) 2SO4•24H2O b.(NH4) 2SO4 c.(NH4) 2CO3.
▼优质解答
答案和解析
废玻璃粉末加氢氧化钠溶液后过滤,得到滤渣A的成分是Fe2O3、CeO2、FeO;滤渣A(Fe2O3、CeO2、FeO)加稀硫酸后过滤得滤液B是硫酸亚铁溶液,加入硫酸和氧化剂过氧化氢可生成溶液C中为硫酸铁,所加氧化剂过氧化氢不引入新杂质,加热蒸发得到溶液D为饱和硫酸铁溶液,在溶液中加入硫酸铵溶液得到硫酸铁铵矾;滤渣B的成分是CeO2;CeO2与H2O2和稀H2SO4反应生成Ce3+和O2,加入HT硫酸萃取,将Ce3+从水溶液中萃取出来,Ce3+加碱和氧气发生氧化还原反应生成Ce(OH)4;
(1)反应①是二氧化硅溶于氢氧化钠溶液中生成硅酸钠和水,反应的离子方程式是:SiO2+2OH-=SiO32-+H2O,
故答案为:SiO2+2OH-=SiO32-+H2O;
(2)反应②中H2O2的作用是氧化使亚铁离子为铁离子,
故答案为:氧化使Fe2+转化为Fe3+;
(3)反应③是酸性溶液中CeO2被过氧化氢还原生成Ce3+离子,过氧化氢被氧化生成氧气,反应的离子方程式:2GeO2+6H++H2O2=2Ge3++4H2O+O2↑,
故答案为:2GeO2+6H++H2O2=2Ge3++4H2O+O2↑;
(4)有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为:2Ce3+(水层)+6HT(有机层)═2CeT3(有机层)+6H+(水层),加入硫酸增大氢离子浓度,平衡逆向进行向形成Ge3+水溶液方向移动,获得较纯的含Ce3+的水溶液;
故答案为:混合液中加入H2SO4使c(H+)增大,平衡向形成Ge3+水溶液方向移动;
(5)硫酸铁铵矾[Fe2(SO4)3•(NH4)2SO4•24H2O]广泛用于水的净化处理,其净水原理是溶解后溶液中的铁离子水解生成氢氧化铁胶体,胶体具有吸附悬浮杂质的作用,可以净水,反应的离子方程式为:Fe3++3H2O=Fe(OH)3+3H+,
故答案为:Fe3++3H2O=Fe(OH)3+3H+;
(6)相同物质的量浓度的以下三种溶液中,a.Fe2(SO4)3•(NH4)2SO4•24H2O 溶液中铁离子水解显酸性抑制铵根离子水解,铵根离子浓度增大;
b.(NH4)2SO4 溶液中硫酸根离子对铵根离子水解无影响;
c.(NH4)2CO3,溶液中碳酸根离子水解显碱性促进铵根离子水解,铵根离子浓度减小;
所以三种溶液中NH4+的浓度由大到小的顺序是:a>b>c,
故答案为:a>b>c.
(1)反应①是二氧化硅溶于氢氧化钠溶液中生成硅酸钠和水,反应的离子方程式是:SiO2+2OH-=SiO32-+H2O,
故答案为:SiO2+2OH-=SiO32-+H2O;
(2)反应②中H2O2的作用是氧化使亚铁离子为铁离子,
故答案为:氧化使Fe2+转化为Fe3+;
(3)反应③是酸性溶液中CeO2被过氧化氢还原生成Ce3+离子,过氧化氢被氧化生成氧气,反应的离子方程式:2GeO2+6H++H2O2=2Ge3++4H2O+O2↑,
故答案为:2GeO2+6H++H2O2=2Ge3++4H2O+O2↑;
(4)有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为:2Ce3+(水层)+6HT(有机层)═2CeT3(有机层)+6H+(水层),加入硫酸增大氢离子浓度,平衡逆向进行向形成Ge3+水溶液方向移动,获得较纯的含Ce3+的水溶液;
故答案为:混合液中加入H2SO4使c(H+)增大,平衡向形成Ge3+水溶液方向移动;
(5)硫酸铁铵矾[Fe2(SO4)3•(NH4)2SO4•24H2O]广泛用于水的净化处理,其净水原理是溶解后溶液中的铁离子水解生成氢氧化铁胶体,胶体具有吸附悬浮杂质的作用,可以净水,反应的离子方程式为:Fe3++3H2O=Fe(OH)3+3H+,
故答案为:Fe3++3H2O=Fe(OH)3+3H+;
(6)相同物质的量浓度的以下三种溶液中,a.Fe2(SO4)3•(NH4)2SO4•24H2O 溶液中铁离子水解显酸性抑制铵根离子水解,铵根离子浓度增大;
b.(NH4)2SO4 溶液中硫酸根离子对铵根离子水解无影响;
c.(NH4)2CO3,溶液中碳酸根离子水解显碱性促进铵根离子水解,铵根离子浓度减小;
所以三种溶液中NH4+的浓度由大到小的顺序是:a>b>c,
故答案为:a>b>c.
看了 废旧显示屏玻璃中含SiO2、...的网友还看了以下:
把上端A封闭、下端B开口的玻璃管插入水中放掉部分空气后放手,玻璃管可以竖直地浮在水中(如下图甲)。 2020-04-07 …
把一端开口一端封闭的玻璃管插入水中(开口向下);玻璃管可竖直地浮在水中.设玻璃管的质量为40克,横 2020-04-07 …
关于原子的玻尔模型,下列说法正确的是()A.原子的能量是连续的B.电子在原子内部静止不动C.电子的 2020-05-14 …
竖直放置的玻璃管下端封闭,上端开口,最上端有一段高h(cm)的水银柱在管中封闭着一段气体.当时大气 2020-05-23 …
艺术长廊有一副玻璃浮雕画,用24块边长5分米的正方形玻璃拼接而成,每一块单独成画,24块玻璃有能组 2020-06-27 …
如图,倒立的玻璃管中蜡块恰能匀速上升,速度为0.1m/s,若在蜡块上升的同时,让玻璃管由静止开始, 2020-07-06 …
Na2CO3溶液能不能保存在带玻璃塞的试剂瓶中?我查过资料,其中解释了NaOH溶液不能保存在带玻璃 2020-07-06 …
在图甲中,闭合开关后,给玻璃珠加热到红炽状态,小灯泡.原因是玻璃变成了.在图乙中,闭合开关后.在给 2020-07-21 …
在现代装修中,要经常使用“毛玻璃”,物体被“毛玻璃”遮住后就看不见了,其原因是()A.物体射向“毛玻 2020-10-30 …
小明看见吸盘能贴在玻璃上产生了疑问,老师告诉他这是大气压把吸盘压在了玻璃上,可小明固执的认为吸盘是粘 2020-12-24 …