早教吧作业答案频道 -->化学-->
硫酸亚铁晶体(FeSO4•7H2O)俗称绿矾,加热至高温会分解.某化学研究小组利用如图装置探究FeSO4分解后的产物.实验步骤:按图组装好仪器(已省略夹持仪器)并检查装置的气密性,准确
题目详情
硫酸亚铁晶体(FeSO4•7H2O)俗称绿矾,加热至高温会分解.某化学研究小组利用如图装置探究FeSO4分解后的产物.
实验步骤:
按图组装好仪器(已省略夹持仪器)并检查装置的气密性,准确称取m gFeSO4固体置于硬质玻璃管中,将E中的导管撤出水槽,打开活塞K,通入一段时间的N2,关闭活塞K.加热A中的玻璃管一段时间后,将E中导管置于水槽集气瓶口收集产生的气体,用带火星的木条检验E中所收集的气体,带火星的木条能够复燃.待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却,得到红棕色粉末.请回答下列问题:
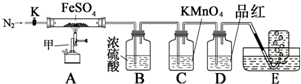
(1)仪器甲的名称是___;
(2)B中浓硫酸的作用___;
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化.写出C中发生反应的离子方程式___;
(4)FeSO4完全分解后,还需要通入一段时间N2的原因是___;
(5)若C中原先加入了20mL 1.00mol/L的KMnO4溶液,为了确定FeSO4分解的化学方程式,某同学进行了如下实验:
I、称量B装置在实验前后增重0.80g;
II、将实验后C中的溶液全部转移至100mL容量瓶中,并加水稀释至刻度线;
III、准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mol/L标准H2C2O4溶液滴定至终点;
IV、重复实验3次,记录数据如表
①滴定至终点的现象___;
②FeSO4分解的化学方程式为___;
(6)请设计一个实验来检验A中的FeSO4是否完全分解___.
实验步骤:
按图组装好仪器(已省略夹持仪器)并检查装置的气密性,准确称取m gFeSO4固体置于硬质玻璃管中,将E中的导管撤出水槽,打开活塞K,通入一段时间的N2,关闭活塞K.加热A中的玻璃管一段时间后,将E中导管置于水槽集气瓶口收集产生的气体,用带火星的木条检验E中所收集的气体,带火星的木条能够复燃.待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却,得到红棕色粉末.请回答下列问题:

(1)仪器甲的名称是___;
(2)B中浓硫酸的作用___;
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化.写出C中发生反应的离子方程式___;
(4)FeSO4完全分解后,还需要通入一段时间N2的原因是___;
(5)若C中原先加入了20mL 1.00mol/L的KMnO4溶液,为了确定FeSO4分解的化学方程式,某同学进行了如下实验:
I、称量B装置在实验前后增重0.80g;
II、将实验后C中的溶液全部转移至100mL容量瓶中,并加水稀释至刻度线;
III、准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mol/L标准H2C2O4溶液滴定至终点;
IV、重复实验3次,记录数据如表
| 实验 | 滴定管开始读数 | 滴定终点读数 |
| 1 | 0 | 19.98 |
| 2 | 0.10 | 20.12 |
| 3 | 0 | 20.16 |
②FeSO4分解的化学方程式为___;
(6)请设计一个实验来检验A中的FeSO4是否完全分解___.
▼优质解答
答案和解析
(1)装置图中仪器甲为酒精喷灯,
故答案为:酒精喷灯;
(2)探究FeSO4分解后的产物依据分析可知,分解产物中有氧气、氧化铁生成,结合氧化还原反应氧元素、铁元素化合价升高,则硫元素化合价降低生成二氧化硫,原子守恒可得到同时会生成三氧化硫,所以B中浓硫酸的作用吸收分解产生的SO3,
故答案为:吸收分解产生的SO3;
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化说明出二氧化硫被高锰酸钾溶液全部吸收,反应的离子方程式为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,
故答案为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
(4)FeSO4完全分解后,还需要通入一段时间N2的原因是将装置内残留的气体排入吸收装置2完全吸收,同时防止发生倒吸,
故答案为:将装置内残留的气体排入吸收装置2完全吸收,同时防止发生倒吸;
(5)准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mol/L标准H2C2O4溶液滴定至终点,是滴定装置C中剩余高锰酸钾,
①高锰酸钾溶液呈紫红色,滴入草酸发生氧化还原反应,反应终点可以依据高锰酸钾溶液颜色判断,滴入最后一滴溶液紫红色变化为无色且半分钟无变化证明反应达到终点,
故答案为:溶液由紫红色变为无色且半分钟不恢复成紫红色;
②3组实验数据误差较大舍去,依据1、2组消耗溶液体积=
=20ml,n(H2C2O4)=0.20mol/L×0.020L=0.004mol,
2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
2 5
n 0.040mol
n=0.0016mol,
装置C中共有剩余高锰酸钾物质的量=0.0016mol×
=0.008mol,与二氧化硫反应的高锰酸钾物质的量=0.020L×1.00mol/L-0.008mol=0.012mol,
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,
5 2
n(SO2) 0.012mol
n(SO2)=0.03mol
称量B装置在实验前后增重0.80g为三氧化硫n(SO3)=
=0.01mol
硫元素降低生成二氧化硫电子转移0.03mol×2=0.06mol,
原子守恒得到反应的FeSO4共0.03mol+0.01mol=0.04mol,
2FeSO4 ~Fe2O3~2e-
2 1 2
0.04mol 0.02mol 0.04mol
FeSO4~O2~4e-
1 4
0.005mol 0.02mol
反应中FeSO4:Fe2O3:SO3:SO2:O2=0.04:0.002:0.01:0.012:0.005=8:4:2:6:1
反应的化学方程式为:8FeSO4
4Fe2O3+2SO3↑+6SO2↑+O2↑,
故答案为:8FeSO4
4Fe2O3+2SO3↑+6SO2↑+O2↑;
(6)检验固体中是否有未分解的硫酸亚铁,设计实验检验剩余固体中是否含亚铁离子,结合亚铁离子的特征检验试剂和反应现象设计,具体步骤为:将废液后的固体转移到小烧杯中,加入少量水搅拌过滤,取少量滤液于试管中,加入几滴K3[Fe(CN)6]溶液,若产生特征蓝色沉淀,说明硫酸亚铁未全部分解,反之则分解完全,
故答案为:将废液后的固体转移到小烧杯中,加入少量水搅拌过滤,取少量滤液于试管中,加入几滴K3[Fe(CN)6]溶液,若产生特征蓝色沉淀,说明硫酸亚铁未全部分解,反之则分解完全.
故答案为:酒精喷灯;
(2)探究FeSO4分解后的产物依据分析可知,分解产物中有氧气、氧化铁生成,结合氧化还原反应氧元素、铁元素化合价升高,则硫元素化合价降低生成二氧化硫,原子守恒可得到同时会生成三氧化硫,所以B中浓硫酸的作用吸收分解产生的SO3,
故答案为:吸收分解产生的SO3;
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化说明出二氧化硫被高锰酸钾溶液全部吸收,反应的离子方程式为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,
故答案为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
(4)FeSO4完全分解后,还需要通入一段时间N2的原因是将装置内残留的气体排入吸收装置2完全吸收,同时防止发生倒吸,
故答案为:将装置内残留的气体排入吸收装置2完全吸收,同时防止发生倒吸;
(5)准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mol/L标准H2C2O4溶液滴定至终点,是滴定装置C中剩余高锰酸钾,
①高锰酸钾溶液呈紫红色,滴入草酸发生氧化还原反应,反应终点可以依据高锰酸钾溶液颜色判断,滴入最后一滴溶液紫红色变化为无色且半分钟无变化证明反应达到终点,
故答案为:溶液由紫红色变为无色且半分钟不恢复成紫红色;
②3组实验数据误差较大舍去,依据1、2组消耗溶液体积=
| 19.98+20.12-0.1 |
| 2 |
2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
2 5
n 0.040mol
n=0.0016mol,
装置C中共有剩余高锰酸钾物质的量=0.0016mol×
| 100 |
| 20 |
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,
5 2
n(SO2) 0.012mol
n(SO2)=0.03mol
称量B装置在实验前后增重0.80g为三氧化硫n(SO3)=
| 0.80g |
| 80g/mol |
硫元素降低生成二氧化硫电子转移0.03mol×2=0.06mol,
原子守恒得到反应的FeSO4共0.03mol+0.01mol=0.04mol,
2FeSO4 ~Fe2O3~2e-
2 1 2
0.04mol 0.02mol 0.04mol
FeSO4~O2~4e-
1 4
0.005mol 0.02mol
反应中FeSO4:Fe2O3:SO3:SO2:O2=0.04:0.002:0.01:0.012:0.005=8:4:2:6:1
反应的化学方程式为:8FeSO4
| ||
故答案为:8FeSO4
| ||
(6)检验固体中是否有未分解的硫酸亚铁,设计实验检验剩余固体中是否含亚铁离子,结合亚铁离子的特征检验试剂和反应现象设计,具体步骤为:将废液后的固体转移到小烧杯中,加入少量水搅拌过滤,取少量滤液于试管中,加入几滴K3[Fe(CN)6]溶液,若产生特征蓝色沉淀,说明硫酸亚铁未全部分解,反之则分解完全,
故答案为:将废液后的固体转移到小烧杯中,加入少量水搅拌过滤,取少量滤液于试管中,加入几滴K3[Fe(CN)6]溶液,若产生特征蓝色沉淀,说明硫酸亚铁未全部分解,反之则分解完全.
看了 硫酸亚铁晶体(FeSO4•7...的网友还看了以下:
统计学问题,已知有40个数据,那么如何确定组数?采用组居分组时,第一步要确定组数K,组数K要在5~ 2020-05-17 …
采用组距分组的步骤有( )。A.确定分组组数B.对原始资料进行排序、求极差C.确定各组组距、确定组限 2020-05-30 …
下列说法不正确的是()A.人体中含量最多的金属元素是钙元素B.球墨铸铁在某些场合可以代替钢C.生铁 2020-06-21 …
有一段用固定镜头拍摄的一列武广高铁动车组视频,小田通过播放该视频来测算机车运行速度.已知机车长度是s 2020-11-08 …
下列说法不正确的是()A.生铁和钢都是由铁元素组成的B.人体中含量最多的金属元素是钙元素C.球墨铸铁 2020-11-20 …
氧化铁是重要工业颜料,以废铁屑为原料制备氧化铁的步骤如下:(部分操作和条件略)步骤1:用碳酸钠溶液洗 2020-12-07 …
氧化铁是重要工业颜料,以废铁屑为原料制备氧化铁的步骤如下:(部分操作和条件略)步骤1:用碳酸钠溶液洗 2020-12-07 …
有一段用固定镜头拍摄的一列武广高铁动车组视频,小田通过播放该视频来测算机车运动速度。已知机车长度是s 2020-12-13 …
(2013•滨湖区一模)无锡地铁1、2号线即将于2014年通车,为了解市民对地铁票的定价意向,市物价 2020-12-15 …
郑州地铁1号线在2013年12月28日通车之前,为了解市民对地铁票的定价意向,市物价局向社会公开征集 2020-12-29 …