早教吧作业答案频道 -->化学-->
草酸(H2C2O4)是一种还原性二元酸,存在于菠菜等植物中.已知常温下,草酸的电离常数K1=5.4×10-2,K2=5.4×10-5.溶度积常数:草酸钙Ksp(CaC2O4)=4.0×10-8,Ksp(CaSO4)=7.10×10-9.
题目详情
草酸(H2C2O4)是一种还原性二元酸,存在于菠菜等植物中.已知常温下,草酸的电离常数K1=5.4×10-2,K2=5.4×10-5.溶度积常数:草酸钙Ksp(CaC2O4)=4.0×10-8,Ksp(CaSO4)=7.10×10-9.请回答下列问题:
(1)生活中,长期将豆腐与菠菜混合食用,容易损失钙素且患胆结石疾病.简述理由:___
(2)写出草酸在水中的电离方程式:___
(3)已知KHC2O4溶液显酸性则溶液中c(H2C2O4)___(填“>”、“<“或“=”,下同)c(C2O42-).若0.1mol•L-1的H2C2O4溶液中第二步电离的c(H+)=amol•L-1,则0.1mol•L-1的KHC2O4溶液中HC2O4-电离出来的c(H+)___amol•L-1
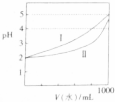
(4)常温下,将1mL某浓度草酸溶液加蒸馏水稀释,其溶液pH与加水稀释后溶液体积关系如图所示.能代表草酸溶液稀释情况的曲线是___(填“Ⅰ”或“Ⅱ”)在稀释该溶液过程中,下列物理量始终增大的是___
A.
B.
C.
D.
.
(5)草酸亚铁是草酸的重要盐类,它是制备高纯度活性铁粉的原料,测定药品纯度步骤如下:准确称取wg草酸亚铁(FeC2O4)样品,将其研磨成粉末(假设杂质不反应),后溶于适量的稀碳酸配制成250mL溶液.准确量取20mL该溶液于容量瓶中,用c1mol•L-1的K2Cr2O7酸性溶液(用稀硫酸酸化)滴定至终点,消耗滴定液VmL,(还原产物为Cr3+,氧化产物为Fe3+和CO2)
①盛装滴定液的滴定管宜选择___(填字母)
A.碱式滴定管 B.酸式滴定管 C.棕色滴定管
②根据上述数据计算,该草酸亚铁样品纯度为___.

(1)生活中,长期将豆腐与菠菜混合食用,容易损失钙素且患胆结石疾病.简述理由:___
(2)写出草酸在水中的电离方程式:___
(3)已知KHC2O4溶液显酸性则溶液中c(H2C2O4)___(填“>”、“<“或“=”,下同)c(C2O42-).若0.1mol•L-1的H2C2O4溶液中第二步电离的c(H+)=amol•L-1,则0.1mol•L-1的KHC2O4溶液中HC2O4-电离出来的c(H+)___amol•L-1
(4)常温下,将1mL某浓度草酸溶液加蒸馏水稀释,其溶液pH与加水稀释后溶液体积关系如图所示.能代表草酸溶液稀释情况的曲线是___(填“Ⅰ”或“Ⅱ”)在稀释该溶液过程中,下列物理量始终增大的是___
A.
| c(H+)•c(HC2O4-) |
| c(H2C2O4) |
| c(H+)•c(C2O42-) |
| c(HC2O42-) |
| c(C2O42-) |
| c(H2C2O4) |
| c(OH-) |
| c(H+) |
(5)草酸亚铁是草酸的重要盐类,它是制备高纯度活性铁粉的原料,测定药品纯度步骤如下:准确称取wg草酸亚铁(FeC2O4)样品,将其研磨成粉末(假设杂质不反应),后溶于适量的稀碳酸配制成250mL溶液.准确量取20mL该溶液于容量瓶中,用c1mol•L-1的K2Cr2O7酸性溶液(用稀硫酸酸化)滴定至终点,消耗滴定液VmL,(还原产物为Cr3+,氧化产物为Fe3+和CO2)
①盛装滴定液的滴定管宜选择___(填字母)
A.碱式滴定管 B.酸式滴定管 C.棕色滴定管
②根据上述数据计算,该草酸亚铁样品纯度为___.
▼优质解答
答案和解析
(1)草酸钙是不能被人体吸收的沉积物,豆腐中含有较多的钙盐,豆腐里的钙盐和菠菜里的草酸容易形成草酸钙,不利于人体吸收,
故答案为:豆腐里的钙盐和菠菜里的草酸容易形成草酸钙,不利于人体吸收;
(2)草酸是二元弱酸,在水溶液里存在两步电离,第一步电离程度大于第二步,其电离方程式分别为:H2C2O4⇌HC2O4-+H+、HC2O4-⇌C2O42-+H+,
故答案为:H2C2O4⇌HC2O4-+H+、HC2O4-⇌C2O42-+H+;
(3)KHC2O4溶液显酸性说明HC2O4-的电离程度大于水解程度,因此c(C2O42-)大于c(H2C2O4),同为0.1mol•L-1的H2C2O4溶液何KHC2O4溶液相比,KHC2O4溶液中氢离子浓度较小,对HC2O4-⇌C2O42-+H+的抑制就小,因此0.1mol•L-1的KHC2O4溶液中HC2O4-电离出来的c(H+)>amol•L-1,
故答案为:<;>;
(4)草酸为二元弱酸,pH=2的草酸溶液,加水稀释1000倍,pH增大不到3个单位,因此能代表草酸溶液稀释情况的曲线是Ⅱ;
稀释过程促进草酸的电离,则
A.
=Ka1,电离平衡常数只受到温度的影响,因此比值始终不变;
B.
=Ka2,电离平衡常数只受到温度的影响,因此比值始终不变;
C.
=
,草酸加水稀释,n(C2O42-)增大,n(H2C2O4)减小,因此比值增大;
D.
,草酸加水稀释,c(H+)减小,由Kw=c(H+)•c(OH-)不变可知c(H+)增大,因此比值增大;
故答案为:Ⅱ;CD;
(5)①K2Cr2O7酸性溶液(用稀硫酸酸化)为酸性、强氧化性溶液,对橡胶造成腐蚀,应使用酸式滴定管,故答案为:B;
②草酸亚铁与重铬酸钾反应K2Cr2O7+2FeC2O4+7H2SO4=Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O+4CO2↑,则
wg草酸亚铁(FeC2O4)样品中含有FeC2O4的物质的量为c1mol•L-1×V×10-3L×2,
质量为c1mol•L-1×V×10-3L×2×
×144g/mol=3.6c1V g,
草酸亚铁样品纯度为
×100%=
%,
故答案为:
%.
故答案为:豆腐里的钙盐和菠菜里的草酸容易形成草酸钙,不利于人体吸收;
(2)草酸是二元弱酸,在水溶液里存在两步电离,第一步电离程度大于第二步,其电离方程式分别为:H2C2O4⇌HC2O4-+H+、HC2O4-⇌C2O42-+H+,
故答案为:H2C2O4⇌HC2O4-+H+、HC2O4-⇌C2O42-+H+;
(3)KHC2O4溶液显酸性说明HC2O4-的电离程度大于水解程度,因此c(C2O42-)大于c(H2C2O4),同为0.1mol•L-1的H2C2O4溶液何KHC2O4溶液相比,KHC2O4溶液中氢离子浓度较小,对HC2O4-⇌C2O42-+H+的抑制就小,因此0.1mol•L-1的KHC2O4溶液中HC2O4-电离出来的c(H+)>amol•L-1,
故答案为:<;>;
(4)草酸为二元弱酸,pH=2的草酸溶液,加水稀释1000倍,pH增大不到3个单位,因此能代表草酸溶液稀释情况的曲线是Ⅱ;
稀释过程促进草酸的电离,则
A.
| c(H+)•c(HC2O4-) |
| c(H2C2O4) |
B.
| c(H+)•c(C2O42-) |
| c(HC2O42-) |
C.
| c(C2O42-) |
| c(H2C2O4) |
| n(C2O42-) |
| n(H2C2O4) |
D.
| c(OH-) |
| c(H+) |
故答案为:Ⅱ;CD;
(5)①K2Cr2O7酸性溶液(用稀硫酸酸化)为酸性、强氧化性溶液,对橡胶造成腐蚀,应使用酸式滴定管,故答案为:B;
②草酸亚铁与重铬酸钾反应K2Cr2O7+2FeC2O4+7H2SO4=Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O+4CO2↑,则
wg草酸亚铁(FeC2O4)样品中含有FeC2O4的物质的量为c1mol•L-1×V×10-3L×2,
质量为c1mol•L-1×V×10-3L×2×
| 250ml |
| 20ml |
草酸亚铁样品纯度为
| 3.6c1Vg |
| wg |
| 360c1V |
| w |
故答案为:
| 360c1V |
| w |
看了 草酸(H2C2O4)是一种还...的网友还看了以下:
简便计算1.1/2+1/4+1/8+1/16+1/32+1/64+1/1282.60又3/5÷12 2020-05-14 …
有一个高为1.1米的正方体水池刚好能装满28桶水,已知水桶是一个圆柱体,...有一个高为1.1米的 2020-05-20 …
一、我们知道1/1×2=1/1-1/2=1/2,1/2×3=1/2-1/3=1/6验证:1/3×4 2020-07-17 …
直角三角形1:1:根号2请问各路高手:直角三角形三个角分别为30°60°90°我想问的是:1:1: 2020-07-22 …
寻找规律解数学题1/1*2=1-1/22/2*3=1/2-1/31/3*4=1/3-1/4……计算 2020-07-22 …
由下列各式:1>1/2,1+1/2+1/3>1有下列各式:1>1/2;1+1/2+1/3>1;1+1 2020-10-30 …
直接写出得数.0.5+0.5÷0.1=8.64×9×0=1.34×8×25=1.8+1.8×4=1- 2020-11-19 …
直接写出得数6.3÷9=4.2÷2.1=8-2.6=4×1.5=0.32+0.8=1.7+0.25= 2020-11-19 …
计算一道数学题,(1+1/2)×(1+1/3)×(1+1/4)×(1+1/5)×(1+1/6)×(1 2020-11-30 …
三元醇F的分子式为C3H6O3,在核磁共振氢谱图中峰值比为4:2:1:1,请问F的结构式是什么?为什 2020-12-31 …