卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子.若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁.若要求产品尽量不含杂质,而且生产成本较
卤块的主要成分是MgCl 2 ,此外还含Fe 3+ 、Fe 2+ 和Mn 2+ 等离子.若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁.
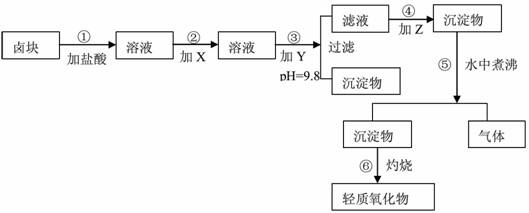
若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,填写空白:
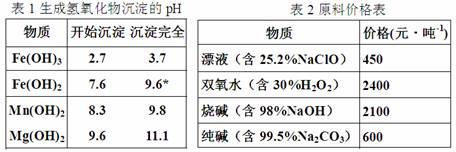
Fe 2+ 氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe 3+ ,生成Fe(OH) 3 沉淀除去.(1)在步骤②中加入的试剂X,最佳的选择是 ,漂液
其作用是
(2)在步骤③中加入的试剂应是 NaOH
;之所以要控制pH=9.8,其目的是
。
(3)在步骤④中加入的试剂Z应是 纯碱
;
(4)在步骤⑤中发生的反应是 。 MgCO 3 +H 2 O=Mg(OH) 2 +CO 2
(5)在实验室中,为了除去MgCl 2 酸性溶液中的Fe 3+ 而得到较纯净的MgCl 2 溶液,可在加热搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量的盐酸,这种试剂是 。
A.NH 3 ·H 2 O B.NaOH C.Na 2 CO 3 D.MgCO 3
(6)已知MgCl 2 ·6H 2 O受热时发生水解:MgCl 2 ·6H 2 O=Mg(OH)Cl+HCl↑+5H 2 O而MgSO 4 ·7H 2 O受热不易发生水解。试解释原因
。
(7)过滤后的沉淀往往需要洗涤,而选择洗涤沉淀的试剂需要考虑沉淀的损失,例如:分别用等体积的蒸馏水和0.010mol/L硫酸洗涤BaSO 4 沉淀, 用水洗涤造成BaSO 4 的损失量大于用稀硫酸洗涤的损失量。试利用平衡移动原理进行解释
。
(1)漂液/NaClO [1分] 将Fe 2+ 氧化为Fe 3+ ; [2分]
(2)烧碱/NaOH [1分] 使Mg 2+ 以外的杂质转化为氢氧化物沉淀除去 [2分]
(3)纯碱/Na 2 CO 3 [1分]
(4)MgCO 3 +H 2 O Mg(OH) 2 +CO 2 ↑ [2分]
Mg(OH) 2 +CO 2 ↑ [2分]
(5)D [1分]
(6)受热时,MgCl 2 •6H 2 O水解反应的生成物HCl逸出反应体系,相当于不断减少可逆反应的生成物,从而使平衡不断向水解反应方向移动;MgSO 4 •7H 2 O没有类似的可促进水解反应进行的情况。 [2分]
(7)硫酸溶液的SO 4 2- 对BaSO 4 的沉淀溶解平衡有促进平衡向生成沉淀的方向移动的作用。 [2分]
卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+和Mn2+等杂质离子.以卤块为原料按下图所示 2020-05-13 …
卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+和Mn2+等杂质离子.以卤块为原料按如图所示 2020-05-13 …
卤块的主要成分是MgCl2,此外还含有少量的Fe3+、Fe2+和Mn2+等离子,以卤块为原料制取轻 2020-05-13 …
如图所示,光滑冰面上原来停着质量为m的物块及总质量M的小孩和冰车已知M:m=16:1,现小孩推物块 2020-06-25 …
7如图所示,质量为M的劈块,静止在水平面上,质量为m的滑块以v0的初速度由底端沿劈块斜面向上运动7 2020-06-28 …
如图所示,小木块质量m=1kg,长木块质量M=10kg,木块与地面以及木块间的动摩擦因数为μ=0.6 2020-10-30 …
一炮弹质量为m,以一定的倾斜角想上发射,到达最高点是速度v,炮弹在最高点爆炸成两块,其中一块沿原轨道 2020-11-10 …
一木块浮在水面上,若将一块质量为6.8kg的铁块A加在这木块上时,刚好使木块浸没,先若将另一块未知质 2020-11-20 …
问到高二动量题以初速度Vo与水平方向成60度角斜向上抛出的手榴弹到达最高点时炸成质量分别为m和2m的 2020-11-30 …
光滑水平面上有一个木板质量为2m一个质量为m的小物块以初速度v与木块左端滑上木块最终恰好在木块右端与 2021-01-17 …