早教吧作业答案频道 -->化学-->
已知某种治疗胃病药品的主要成份是铝碳酸镁片,化学式为AlaMgb(OH)16CO3•4H2O,假设药品中的其它成份受热不分解、不溶于水且不与稀硫酸反应.某研究性学习小组设计了如图一实验探究
题目详情
已知某种治疗胃病药品的主要成份是铝碳酸镁片,化学式为AlaMgb(OH)16CO3•4H2O,假设药品中的其它成份受热不分解、不溶于水且不与稀硫酸反应.某研究性学习小组设计了如图一实验探究铝碳酸镁片的组成.
【实验一】
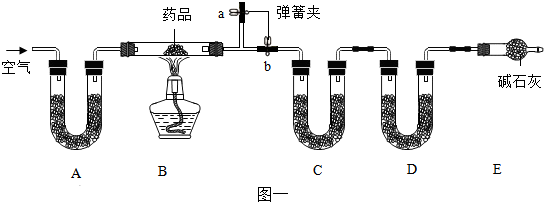
取m g该药片,研成粉末放入硬质玻璃管中,加热,充分反应后测得装置C增重2.16g,装置D增重0.44g.
(1)铝碳酸镁片加热分解的产物为Al2O3、MgO、CO2和水,则为分别测定CO2和水的质量,装置C和D中盛放的药品应选择:C___ D___(填序号).
①浓硫酸 ②碱石灰 ③氯化钙 ④纯碱
(2)实验开始前先通入一定量空气,其操作方法是关闭弹簧夹___,打开弹簧夹___,目的是___.
(3)一段时间后,打开弹簧夹___,关闭弹簧夹___,点燃酒精灯加热,充分反应后,停止加热,继续通入空气至玻璃管冷却的目的是___(填序号).
①排净空气防爆炸 ②防止空气中水和二氧化碳进入C、D影响测定
③使生成水和二氧化碳进入C、D被充分吸收
【实验二】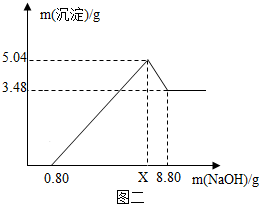
另取m g该药片,加入100g 9.8%的稀硫酸,充分反应后滤去不溶物,得到含有MgSO4和Al2(SO4)3等溶质的滤液,向滤液中逐渐加入足量的稀NaOH溶液,产生沉淀的物质的质量与加入NaOH质量的关系如图二.
已知:MgSO4+2NaOH═Mg(OH)2↓+Na2SO4Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4
Al(OH)3+NaOH═NaAlO2+2H2O,
Mg(OH)2不溶于NaOH,NaAlO2可溶于水.
(1)图中NaOH加入0.80g,仍没有沉淀,说明滤液中含___.当加入NaOH的质量到x时,生成的沉淀有___和___,其中Al(OH)3的质量是___g,则x=___g.
(2)有医生建议患有严重胃溃疡的患者最好慎用该药,试用你所学的知识解释这样建议的理由是___.
(3)试确定铝碳酸镁的化学式为___.

【实验一】
取m g该药片,研成粉末放入硬质玻璃管中,加热,充分反应后测得装置C增重2.16g,装置D增重0.44g.
(1)铝碳酸镁片加热分解的产物为Al2O3、MgO、CO2和水,则为分别测定CO2和水的质量,装置C和D中盛放的药品应选择:C___ D___(填序号).
①浓硫酸 ②碱石灰 ③氯化钙 ④纯碱
(2)实验开始前先通入一定量空气,其操作方法是关闭弹簧夹___,打开弹簧夹___,目的是___.
(3)一段时间后,打开弹簧夹___,关闭弹簧夹___,点燃酒精灯加热,充分反应后,停止加热,继续通入空气至玻璃管冷却的目的是___(填序号).
①排净空气防爆炸 ②防止空气中水和二氧化碳进入C、D影响测定
③使生成水和二氧化碳进入C、D被充分吸收
【实验二】

另取m g该药片,加入100g 9.8%的稀硫酸,充分反应后滤去不溶物,得到含有MgSO4和Al2(SO4)3等溶质的滤液,向滤液中逐渐加入足量的稀NaOH溶液,产生沉淀的物质的质量与加入NaOH质量的关系如图二.
已知:MgSO4+2NaOH═Mg(OH)2↓+Na2SO4Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4
Al(OH)3+NaOH═NaAlO2+2H2O,
Mg(OH)2不溶于NaOH,NaAlO2可溶于水.
(1)图中NaOH加入0.80g,仍没有沉淀,说明滤液中含___.当加入NaOH的质量到x时,生成的沉淀有___和___,其中Al(OH)3的质量是___g,则x=___g.
(2)有医生建议患有严重胃溃疡的患者最好慎用该药,试用你所学的知识解释这样建议的理由是___.
(3)试确定铝碳酸镁的化学式为___.
▼优质解答
答案和解析
实验一、
(1)分析本题的实验装置可知,样品铝碳酸镁片在加热条件下分解生成铝和镁的氧化物、CO2、H2O,装置C中应放入能吸水的物质,但不能吸收二氧化碳气体,否则无法确定生成的水和二氧化碳各自的质量,所以装置C中是吸收水蒸气,利用无水CaCl2或P2O5 可以吸收,装置D是吸收二氧化碳气体的装置,可以利用碱石灰吸收二氧化碳气体,故为:CaCl2; 碱石灰;
(2)实验开始前先通入一段时间空气,气目的是赶净装置B中的二氧化碳和水蒸气,确保CD两装置吸收的水蒸气、二氧化碳全部是样品分解生成的;
(3)所以通入的空气必须先除去空气中的水和二氧化碳A装置中应放入碱石灰或固体氢氧化钠,实验开始前先通入一段时间空气,其目的是排除装置B中的CO2、H2O,其操作方法是;关闭弹簧夹b,打开弹簧夹a;当B处的酒精灯点燃后以及反应结束后一段时间内仍然要通入空气的目的是排出固体分解产生的CO2、H2O,使其被充分吸收,其操作方法是;关闭弹簧夹b,打开弹簧夹a;
实验二、
(1)由图象分析,NaOH加入0.80g,仍没有沉淀,说明滤液含硫酸,当加入NaOH的质量到x时,生成的沉淀有氢氧化镁和氢氧化铝;图象分析沉淀3.48g为Mg(OH)2,Al(OH)3的质量量为5.04-3.48g=1.56g;
设与硫酸镁反应的氢氧化钠的质量为x,与硫酸铝反应的氢氧化钠的质量为y,x
MgSO4+2NaOH═Mg(OH)2↓+Na2SO4 Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4
80 58 240 156
x 3.48g y 1.56g
=
=
x=4.8g y=2.4g
则x=4.8g+2.4g+0.8g=8g;
(2)胃酸主要成分是盐酸,和该药反应生成的二氧化碳容易使胃壁穿孔,故答案为:因为胃酸和该药作用产生CO2会刺激胃粘膜,导致胃穿孔;
(3)根据质量守恒定律,反应前后元素的质量不变,根据以上数据,3.48gMg(OH)2中镁元素的质量为1.44g,原子个数为6个,Al(OH)3的质量量1.56g,铝元素的质量为0.54g,原子个数为2个,
故铝碳酸镁的化学式为Al2Mg6(OH)16CO3•4H2O
答案:实验一、
(1)③②;
(2)b; a; 排尽空气防干扰;
(3)b;a;③;
实验二、
(1)H2SO4 ;Mg(OH)2;Al(OH)3;1.56;8;
(2)与胃中盐酸反应产生CO2,加重病情或造成胃穿孔、胃出血
(3)Al2Mg6(OH)16CO3•4H2O;
实验一、
(1)分析本题的实验装置可知,样品铝碳酸镁片在加热条件下分解生成铝和镁的氧化物、CO2、H2O,装置C中应放入能吸水的物质,但不能吸收二氧化碳气体,否则无法确定生成的水和二氧化碳各自的质量,所以装置C中是吸收水蒸气,利用无水CaCl2或P2O5 可以吸收,装置D是吸收二氧化碳气体的装置,可以利用碱石灰吸收二氧化碳气体,故为:CaCl2; 碱石灰;
(2)实验开始前先通入一段时间空气,气目的是赶净装置B中的二氧化碳和水蒸气,确保CD两装置吸收的水蒸气、二氧化碳全部是样品分解生成的;
(3)所以通入的空气必须先除去空气中的水和二氧化碳A装置中应放入碱石灰或固体氢氧化钠,实验开始前先通入一段时间空气,其目的是排除装置B中的CO2、H2O,其操作方法是;关闭弹簧夹b,打开弹簧夹a;当B处的酒精灯点燃后以及反应结束后一段时间内仍然要通入空气的目的是排出固体分解产生的CO2、H2O,使其被充分吸收,其操作方法是;关闭弹簧夹b,打开弹簧夹a;
实验二、
(1)由图象分析,NaOH加入0.80g,仍没有沉淀,说明滤液含硫酸,当加入NaOH的质量到x时,生成的沉淀有氢氧化镁和氢氧化铝;图象分析沉淀3.48g为Mg(OH)2,Al(OH)3的质量量为5.04-3.48g=1.56g;
设与硫酸镁反应的氢氧化钠的质量为x,与硫酸铝反应的氢氧化钠的质量为y,x
MgSO4+2NaOH═Mg(OH)2↓+Na2SO4 Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4
80 58 240 156
x 3.48g y 1.56g
| 80 |
| x |
| 58 |
| 3.48g |
| 240 |
| y |
| 156 |
| 1.56g |
x=4.8g y=2.4g
则x=4.8g+2.4g+0.8g=8g;
(2)胃酸主要成分是盐酸,和该药反应生成的二氧化碳容易使胃壁穿孔,故答案为:因为胃酸和该药作用产生CO2会刺激胃粘膜,导致胃穿孔;
(3)根据质量守恒定律,反应前后元素的质量不变,根据以上数据,3.48gMg(OH)2中镁元素的质量为1.44g,原子个数为6个,Al(OH)3的质量量1.56g,铝元素的质量为0.54g,原子个数为2个,
故铝碳酸镁的化学式为Al2Mg6(OH)16CO3•4H2O
答案:实验一、
(1)③②;
(2)b; a; 排尽空气防干扰;
(3)b;a;③;
实验二、
(1)H2SO4 ;Mg(OH)2;Al(OH)3;1.56;8;
(2)与胃中盐酸反应产生CO2,加重病情或造成胃穿孔、胃出血
(3)Al2Mg6(OH)16CO3•4H2O;
看了已知某种治疗胃病药品的主要成份...的网友还看了以下:
如果直线y=2x+m与直角坐标系两坐标系围成的三角形面积为4,m=±4这是为什么 2020-04-25 …
a是b的百分之八十.ab两个数字的和是5.4,a是多少?2.一个数字的五分之一是比它的百分之二十五 2020-05-14 …
m^4=81是二项方程吗 2020-06-03 …
大家知道怎么测氢气纯度.我知道一种方法是用奥斯分析仪测定,测的氧气的纯度X就能算出氢气的纯度M.公 2020-06-06 …
A是由2002个“4”组成的多位数,即2002个4.A是不是某个自然数B的平方?如果是,写出B;如 2020-06-06 …
对称点的规律点A(m,n)关于直线y=x+a的对称点的坐标是什么?m,n,a是常数. 2020-06-14 …
当m为何值时,函数y=-(m-2)x^m^2-3+(m-4)是正比例函数? 2020-06-23 …
1*3分之1+3*5分之1……+99*101分之1a的位置是(1,1),()中m、n两点m 到a是 2020-06-27 …
(2) 若函数Y=(M-4)X是关于X的正比例函数,求M的值 2020-06-27 …
一个矩阵秩的问题老师,请问这个怎么理解?因为AB=C,所以r(AB)≤r(A),即r(A)≥r(C 2020-06-30 …