早教吧作业答案频道 -->化学-->
黄铜是Zn以主要添加元素的铜合金.黄铜渣中约含Zn7%、ZnO31%、Cu50%、CuO5%,其余为杂质.处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):已知:ZnO+H2SO4═ZnSO4+H2
题目详情
黄铜是Zn以主要添加元素的铜合金.黄铜渣中约含Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质.处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):
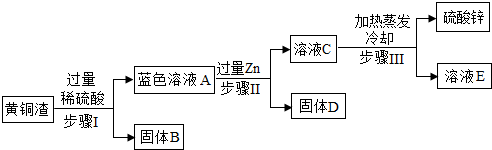
已知:ZnO+H2SO4═ZnSO4+H2O; CuO+H2SO4═CuSO4+H2O
(1)步骤Ⅰ中产生气体的化学方程式为___.
(2)溶液A中的金属阳离子有___(填符号)
(3)步骤Ⅰ、Ⅱ中均包含的操作名称为___,此操作和步骤Ⅲ中的蒸发操作都要用到的玻璃仪器是___.
(4)溶液A___(填“大于”、“小于”或“等于”)溶液C的质量.

已知:ZnO+H2SO4═ZnSO4+H2O; CuO+H2SO4═CuSO4+H2O
(1)步骤Ⅰ中产生气体的化学方程式为___.
(2)溶液A中的金属阳离子有___(填符号)
(3)步骤Ⅰ、Ⅱ中均包含的操作名称为___,此操作和步骤Ⅲ中的蒸发操作都要用到的玻璃仪器是___.
(4)溶液A___(填“大于”、“小于”或“等于”)溶液C的质量.
▼优质解答
答案和解析
(1)氧化锌和氧化铜分别与稀硫酸反应生成硫酸锌、硫酸铜和水,没有气体产生;而锌与稀硫酸反应生成硫酸锌和氢气,化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(2)锌与稀硫酸反应生成硫酸锌和氢气,氧化锌与硫酸反应生成硫酸锌和水,氧化铜与硫酸反应生成硫酸铜和水,其中的金属阳离子是锌离子和铜离子;
(3)由图可知,操作Ⅰ过滤除去铜和杂质,操作Ⅱ过滤是除去锌和置换出的铜;过滤和蒸发操作中均用到玻璃棒这种玻璃仪器,故填:过滤、玻璃棒;
(4)A到C的过程中发生的反应是:Zn+CuSO4=Cu+ZnSO4,
160 161
由此可见溶液的质量增重了.
故答案为:(1)Zn+H2SO4═ZnSO4+H2↑;
(2)Cu2+、Zn2+;
(3)过滤、玻璃棒;
(4)小于.
(2)锌与稀硫酸反应生成硫酸锌和氢气,氧化锌与硫酸反应生成硫酸锌和水,氧化铜与硫酸反应生成硫酸铜和水,其中的金属阳离子是锌离子和铜离子;
(3)由图可知,操作Ⅰ过滤除去铜和杂质,操作Ⅱ过滤是除去锌和置换出的铜;过滤和蒸发操作中均用到玻璃棒这种玻璃仪器,故填:过滤、玻璃棒;
(4)A到C的过程中发生的反应是:Zn+CuSO4=Cu+ZnSO4,
160 161
由此可见溶液的质量增重了.
故答案为:(1)Zn+H2SO4═ZnSO4+H2↑;
(2)Cu2+、Zn2+;
(3)过滤、玻璃棒;
(4)小于.
看了黄铜是Zn以主要添加元素的铜合...的网友还看了以下:
z的模-z的共扼复数=2-4i,求复数z要过程要过程! 2020-03-30 …
{2x+3y-z=10{x-y+z=3注:x.y.z.为互不相等的正整数求3x-y/zx.y.z.为 2020-03-30 …
隐函数求导 设f可微,且方程y+z=xf(y^2-z^2)确定了函数z=z(x,y),隐函数求导 2020-05-16 …
一道复变函数题用级数展开法指出6sinz^3+z^3(z^6-6)在z=0处零点的级要过程啊z^3 2020-06-12 …
溶解过程中放出大量的热的物质:(要化学式和名称)——(),______(),所以稀释浓硫酸要--_ 2020-06-27 …
设变换为u=x-2y、v=x+ay,可把方程d²z/dx²+d²z/(dxdy)-d²z/dy²= 2020-07-09 …
求解方程(z+1)^n=(z-1)^n(n>1,n为自然数)求解方程(z+1)^n=(z-1)^n 2020-07-14 …
三元一次方程要列方程(1)x+2y+z=82x-y-z=-33x+y-2z=-1(2)x+2y+3z 2020-10-31 …
三元一次方程要过程x+y-z=11①y+z-x=5②z+x-y=1③x-y-z=0①x+y-3z=4 2020-10-31 …
X、Y、Z、W是浓度均为0.01mol/L的溶液,其溶质分别是HCl、NH4Cl、NaOH、NaF中 2021-02-01 …