早教吧作业答案频道 -->化学-->
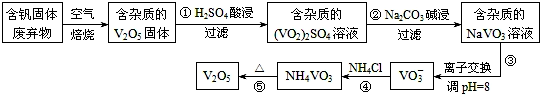
钒是一种重要的合金元素,还用于催化剂和新型电池.从含钒固体废弃物(含有SiO2、Al2O3及其他残渣)中提取钒的一种新工艺主要流程如图:部分含钒化合物在水中的溶解性如表:物质
题目详情
钒是一种重要的合金元素,还用于催化剂和新型电池.从含钒固体废弃物(含有SiO2、Al2O3及其他残渣)中提取钒的一种新工艺主要流程如图:
部分含钒化合物在水中的溶解性如表:
请回答下列问题:
(1)反应①所得溶液中除H+之外的阳离子有___.
(2)反应②碱浸后滤出的固体主要成分是___(写化学式).
(3)反应④的离子方程式为___.
(4)25℃、101kPa时,4Al(s)+3O2(g)═2Al2O3(s)△H1=-a kJ/mol
4V(s)+5O2(g)═2V2O5(s)△H2=-b kJ/mol
用V2O5发生铝热反应冶炼金属钒的热化学方程式是___.
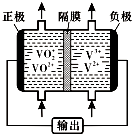
(5)钒液流电池(如图所示)具有广阔的应用领域和市场前景,该电池中隔膜只允许H+通过.电池放电时负极的电极反应式为___,电池充电时阳极的电极反应式是___.
(6)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应①后溶液中的含钒量,反应的离子方程式为:2VO2++H2C2O4+2H+═2VO2++2CO2↑+2H2O.取25.00mL 0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0mL,由此可知,该(VO2)2SO4溶液中钒的含量为___g/L.

部分含钒化合物在水中的溶解性如表:
| 物质 | V2O5 | NH4VO3 | VOSO4 | (VO2)2SO4 |
| 溶解性 | 难溶 | 难溶 | 可溶 | 易溶 |
(1)反应①所得溶液中除H+之外的阳离子有___.
(2)反应②碱浸后滤出的固体主要成分是___(写化学式).
(3)反应④的离子方程式为___.
(4)25℃、101kPa时,4Al(s)+3O2(g)═2Al2O3(s)△H1=-a kJ/mol
4V(s)+5O2(g)═2V2O5(s)△H2=-b kJ/mol
用V2O5发生铝热反应冶炼金属钒的热化学方程式是___.
(5)钒液流电池(如图所示)具有广阔的应用领域和市场前景,该电池中隔膜只允许H+通过.电池放电时负极的电极反应式为___,电池充电时阳极的电极反应式是___.

(6)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应①后溶液中的含钒量,反应的离子方程式为:2VO2++H2C2O4+2H+═2VO2++2CO2↑+2H2O.取25.00mL 0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0mL,由此可知,该(VO2)2SO4溶液中钒的含量为___g/L.
▼优质解答
答案和解析
(1)用硫酸溶解含钒固体废弃物(含有SiO2、Al2O3及其他残渣),生成(VO2)2SO4和硫酸铝,溶液中的阳离子除氢离子外还有VO2+和Al3+,
故答案为:VO2+和Al3+;
(2)含杂质的(VO2)2SO4溶液用碳酸钠溶液碱浸生成含杂质的NaVO3溶液,Al(OH)3不溶于弱碱,所以反应②碱浸后滤出的固体主要成分是Al(OH)3,
故答案为:Al(OH)3;
(3)据工艺流程图可知,反应④的离子方程式为VO3-+NH4+=NH4VO3,故答案为:VO3-+NH4+=NH4VO3↓;
(4)已知①4Al(s)+3O2(g)═2Al2O3(s)△H1=-a kJ/mol
②4V(s)+5O2(g)═2V2O5(s)△H2=-b kJ/mol
据盖斯定律,(①×5-②×3)÷2得:10Al(s)+3V2O5(s)=5Al2O3(s)+6V(s)△H=-
KJ/mol,
故答案为:10Al(s)+3V2O5(s)=5Al2O3(s)+6V(s)△H=-
KJ/mol;
(5)钒液流电池放电时负极发生氧化反应,据图可知,电极反应式为V2+-e-=V3+,正极发生还原反应,充电时,阳极发生氧化反应,电极反应式为VO2+-e-+H2O=VO2++2H+,
故答案为:V2+-e-=V3+;VO2+-e-+H2O=VO2++2H+;
(6)据滴定数据,结合离子方程式c(VO2+)=
=0.2083mol/L,所以1L溶液中含V的质量为0.2083mol/L×1L×51g/mol=10.6g,
故答案为:10.6.
故答案为:VO2+和Al3+;
(2)含杂质的(VO2)2SO4溶液用碳酸钠溶液碱浸生成含杂质的NaVO3溶液,Al(OH)3不溶于弱碱,所以反应②碱浸后滤出的固体主要成分是Al(OH)3,
故答案为:Al(OH)3;
(3)据工艺流程图可知,反应④的离子方程式为VO3-+NH4+=NH4VO3,故答案为:VO3-+NH4+=NH4VO3↓;
(4)已知①4Al(s)+3O2(g)═2Al2O3(s)△H1=-a kJ/mol
②4V(s)+5O2(g)═2V2O5(s)△H2=-b kJ/mol
据盖斯定律,(①×5-②×3)÷2得:10Al(s)+3V2O5(s)=5Al2O3(s)+6V(s)△H=-
| 5a-3b |
| 2 |
故答案为:10Al(s)+3V2O5(s)=5Al2O3(s)+6V(s)△H=-
| 5a-3b |
| 2 |
(5)钒液流电池放电时负极发生氧化反应,据图可知,电极反应式为V2+-e-=V3+,正极发生还原反应,充电时,阳极发生氧化反应,电极反应式为VO2+-e-+H2O=VO2++2H+,
故答案为:V2+-e-=V3+;VO2+-e-+H2O=VO2++2H+;
(6)据滴定数据,结合离子方程式c(VO2+)=
| 2×25.0mL×0.100mol/L |
| 24.0mL |
故答案为:10.6.
看了钒是一种重要的合金元素,还用于...的网友还看了以下:
如图所示为两种育种方法的过程,有关说法正确的是()A.基因重组只发生在图示①③过程中B.借助过程③ 2020-06-13 …
某公司生产一种环保产品,需要添加一种新型原料,若每件产品的利润与新型原料价格成一次函数关系,且每件 2020-06-18 …
近日,在上海街头出现了一种新型垃圾桶,就是运用新技术将废弃的纸、塑料、铝复合软包装等合成后制成的。 2020-06-27 …
节约能源是全社会的一项共同任务,在生活中循环利用废弃物是节约资源的有效途径。目前,在一些城市街头出 2020-06-27 …
稀土是一种不可再生的战略性资源,被广泛应用于电子信息、国防军工等多个领域.一种从废弃阴极射线管(C 2020-07-10 …
钒是一种重要的合金元素,还用于催化剂和新型电池.从含钒固体废弃物(含有SiO2、Al2O3及其他残渣 2020-11-20 …
学校要为图书室新添两种“朝阳读书计划”新书,每种4套.第一种书每套158元,第二种新书每套33元.一 2020-12-05 …
随着科技发展,各种新式地图不断出现,很多人在车上或手机上安装了导航仪,借助导航中提供的清晰地图,方便 2020-12-05 …
大多数明清之际的思想家,对传统价值观进行全面反思和批判的同时,积极倡导一种新的思想,试图为社会提供一 2020-12-12 …
大多数明清之际的思想家,对传统价值观进行全面反思和批判的同时,积极倡导一种新的思想,试图为社会提供一 2020-12-15 …