早教吧作业答案频道 -->化学-->
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:该实验的主要操作步骤如下:①.配制0.20mol/L的盐酸溶液;②.用
题目详情
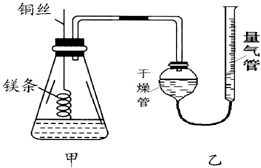
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:
该实验的主要操作步骤如下:
①.配制 0.20mol/L的盐酸溶液;
②.用___量取10.00mL 0.20mol/L的盐酸溶液加入锥形瓶中;
③.用电子天平称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为___;
④.按上图连接好装置,检查装置的气密性;由量气管向干燥管中加适量的水并读出量气管中水面刻度为V1mL(量气管结构类似碱式滴定管).
⑤.反应结束后待体系温度恢复到室温,读出量气管中水面刻度为V2mL.
根据上述步骤提供的信息回答下列问题:
(1)若用密度为1.25g•cm-3,质量分数为36.5%的浓盐酸配制240mL0.20mol/L的盐酸溶液,浓盐酸的溶质的物质的量浓度为___,需这样的浓盐酸___mL.
(2)将上述步骤补充完整:②___;③___.
(3)实验步骤⑤中应选用___(填序号)的量气管.
A.20mL B.50mL C.100mL
读数时除恢复到室温外,还要注意___.
(4)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的为Vm=___,若未除去镁条表面的氧化膜,则测量结果___(填“偏大”、“偏小”或“无影响”).
该实验的主要操作步骤如下:
①.配制 0.20mol/L的盐酸溶液;
②.用___量取10.00mL 0.20mol/L的盐酸溶液加入锥形瓶中;
③.用电子天平称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为___;
④.按上图连接好装置,检查装置的气密性;由量气管向干燥管中加适量的水并读出量气管中水面刻度为V1mL(量气管结构类似碱式滴定管).
⑤.反应结束后待体系温度恢复到室温,读出量气管中水面刻度为V2mL.
根据上述步骤提供的信息回答下列问题:

(1)若用密度为1.25g•cm-3,质量分数为36.5%的浓盐酸配制240mL0.20mol/L的盐酸溶液,浓盐酸的溶质的物质的量浓度为___,需这样的浓盐酸___mL.
(2)将上述步骤补充完整:②___;③___.
(3)实验步骤⑤中应选用___(填序号)的量气管.
A.20mL B.50mL C.100mL
读数时除恢复到室温外,还要注意___.
(4)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的为Vm=___,若未除去镁条表面的氧化膜,则测量结果___(填“偏大”、“偏小”或“无影响”).
▼优质解答
答案和解析
(1)根据公式计算浓盐酸的物质的量浓度,c浓=
×103=
×103=12.5mol/L,容量瓶没有240mL的规格,需要配制250mL,据稀释定律:c浓×V浓=c稀×V稀,则V浓=
=4.00mL,
故答案为:12.5mol/L;4.00;
(2)②题中要求酸的体积10.00 mL较精确,应选酸式滴定管,如用碱式滴定管会腐蚀橡胶管,
故答案为:酸式滴定管;
③Mg+2HCl═MgCl2+H2↑
24g 2 mol
a 0.2mol/L×0.01L
a=0.024 g,
故答案为:0.024;
(3)Mg+2HCl═MgCl2+H2↑
24g 1mol
0.024g n(H2)
完全反应产生氢气的物质的量为n(H2)=0.001mol,在标况下V(H2)=0.001mol×22.4L/mol=0.024L=24mL,在同压、同物质的量的条件下,气体的体积随温度升高而增大,
=
,则室温下的体积V室=
=
=26mL,应选50mL量筒;读数时要保持左右气体压强相等,以减少误差,故应注意:调节量气管高度,使量气管内的液面与干燥管内的液面相平,
故答案为:B;调节量气管高度,使量气管内的液面与干燥管内的液面相平;
(4)若忽略水蒸气的影响,则在该实验条件下测得气体摩尔体积的计算式为Vm=
=
=(V2-V1)L/mol,若未除去镁条表面的氧化膜,导致生成的氢气体积减少,则测量结果偏小,
故答案为:(V2-V1)L/mol;偏小.
| ρω |
| M |
| 1.25×36.5% |
| 36.5 |
| 250mL×0.20mol/L |
| 12.5mol/L |
故答案为:12.5mol/L;4.00;
(2)②题中要求酸的体积10.00 mL较精确,应选酸式滴定管,如用碱式滴定管会腐蚀橡胶管,
故答案为:酸式滴定管;
③Mg+2HCl═MgCl2+H2↑
24g 2 mol
a 0.2mol/L×0.01L
a=0.024 g,
故答案为:0.024;
(3)Mg+2HCl═MgCl2+H2↑
24g 1mol
0.024g n(H2)
完全反应产生氢气的物质的量为n(H2)=0.001mol,在标况下V(H2)=0.001mol×22.4L/mol=0.024L=24mL,在同压、同物质的量的条件下,气体的体积随温度升高而增大,
| V标 |
| V室 |
| T标 |
| T室 |
| V标×T室 |
| T标 |
| 24mL×(273+25)K |
| 273K |
故答案为:B;调节量气管高度,使量气管内的液面与干燥管内的液面相平;
(4)若忽略水蒸气的影响,则在该实验条件下测得气体摩尔体积的计算式为Vm=
| V |
| n |
| (V2-V1)×10-3L |
| 0.001mol |
故答案为:(V2-V1)L/mol;偏小.
看了某研究性学习小组欲测定室温下(...的网友还看了以下:
umol/l,mmol/l换算关系1umol/l=多少mmol/l毫摩尔每升→mmol/L,微摩尔 2020-06-12 …
4、25℃、浓度均为0.1mol/L的下列溶液中c(H+)由大到小的排列顺序:①氨水②NaOH③盐 2020-06-15 …
一支长为L0的蜡烛低部粘一小块铁板,使蜡烛能直立在水中如图所示,蜡烛露出水面的高度为h,现将蜡烛点 2020-07-06 …
如图所示,三根细线于O点处打结,A、B两端固定在同一水平面上相距为L的两点上,使AOB成直角三角形 2020-07-20 …
如图所示,三根细线在O点处打结,A、B端固定在同一水平面上相距为l的两点上,使AOB成直角三角形, 2020-07-24 …
概率统计问题,急,推广的二项系数公式(-r,L)=(-1)^L(r+L-1,L)怎么得来的?∞∑( 2020-07-30 …
长度为L的矩形板,以速度v沿光滑的水平面平动时,垂直滑向宽度为l的粗糙地带,板从开始受阻到停下来,所 2020-11-22 …
两人在空腹状态下,同时一次性口服葡萄糖100克,然后每隔l小时测定一次血糖舍量,将结果绘成如图曲线. 2020-12-04 …
相同PH的弱酸和强酸被不同体积的水稀释后PH仍然一样那么所用体积是否一样?还有将0.1mol·L-1 2020-12-09 …
在常温常压下,向10mL&小bsp;0.01mol/L&小bsp;4eCl3溶液中滴入1mL&小bs 2020-12-15 …