早教吧作业答案频道 -->化学-->
已知Na2S2O3溶液与Cl2反应时,1molNa2S2O3转移8mol电子.该反应的离子方程式是.甲同学设计如图实验流程探究Na2S2O3的化学性质.(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和
题目详情
已知Na2S2O3溶液与Cl2反应时,1mol Na2S2O3转移8mol电子.该反应的离子方程式是___.
甲同学设计如图实验流程探究Na2S2O3的化学性质.
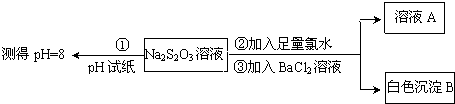
(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和___性.
(Ⅱ)加入BaCl2溶液生成白色沉淀B的离子方程式是___.
(Ⅲ)乙同学认为应将上述流程中②③所加试剂顺序颠倒,你认为甲、乙两同学的设计更合理的是___(填“甲”或“乙”),理由是___.
甲同学设计如图实验流程探究Na2S2O3的化学性质.

(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和___性.
(Ⅱ)加入BaCl2溶液生成白色沉淀B的离子方程式是___.
(Ⅲ)乙同学认为应将上述流程中②③所加试剂顺序颠倒,你认为甲、乙两同学的设计更合理的是___(填“甲”或“乙”),理由是___.
▼优质解答
答案和解析
氯气有强氧化性,能将S2O32-氧化为SO42-,每消耗1mol Na2S2O3转移8mol e-,根据电子转移守恒,可知S2O32-被氧化生成SO42-,而而Cl2被还原为Cl-离子,配平可得离子方程式为:S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+,故答...
看了已知Na2S2O3溶液与Cl2...的网友还看了以下:
设f(x)=lnx−x−ax(其中a>0),g(x)=2(x−1)−(x2+1)lnx.(1)当x 2020-05-13 …
以下不属于供应链设计中需要注意的要点是(2)。A.具有相关性和整体性B.安全性和动态性C.结构性和有 2020-05-26 …
由y=f(x)的参数方程求其单调性和凹凸性时,方法一般是将参数方程求一阶导数和二阶导数,即dy/d 2020-06-16 …
设a1=(1,1,1)T,a2=(1,2,3)T,a3=(1,3,t)T.(1)问t为何值时,向量 2020-07-22 …
真理相对性和绝对性统一的原理用以说明社会主义建设必须坚定不移坚持和发展马克思2.试述真理相对性和绝 2020-07-22 …
请完成以下设计实验,验证根的向重力性和茎的背重力性。(9分)(1)原理分析重力→→→→(2)实验设 2020-07-24 …
线性代数线性相关性的问题~设非零向量β可由α1,α2,……,αr线性表示,但不能由α1,α2,…… 2020-07-31 …
某研究性学习小组根据氧化还原反应规律,欲探究NO2、NO与Na2O2反应的情况.I.从理论上分析,N 2020-11-07 …
为了探究Cu(NO3)2的氧化性和热稳定性,某化学兴趣小组设计了如下实验.回答下列问题:Ⅰ.Cu(N 2020-11-25 …
2006年第2期《求是》载文指出,党的先进性建设是关系马克思主义政党生存发展的根本性问题,也是加强和 2020-11-27 …