早教吧作业答案频道 -->化学-->
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程.烧瓶C中发生反应如下:Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)(Ⅰ)2H2S(aq)+S
题目详情
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程.
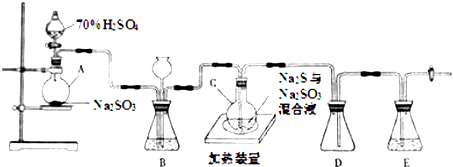
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)
Na2S2O3(aq) (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若___,则整个装置气密性良好.装置D的作用是___.装置E中为___溶液.
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为___.
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择___.
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:___.
已知Na2S2O3•5H2O遇酸易分 S2O32‾+2H+=S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.

烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)
| ||
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若___,则整个装置气密性良好.装置D的作用是___.装置E中为___溶液.
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为___.
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择___.
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:___.
已知Na2S2O3•5H2O遇酸易分 S2O32‾+2H+=S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.
▼优质解答
答案和解析
A中硫酸和亚硫酸钠反应生成SO2,装置B的作用之一是观察SO2的生成速率,B装置不能吸收SO2,则B中含有盛放饱和的NaHSO3溶液,C中在加热条件下发生反应Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)、2H2S(aq)+SO2(g)=3S(s)+2H2O、S(s)+Na2SO3(aq)
Na2S2O3(aq),D对于E来说有缓冲作用,能防止E中发生倒吸现象,二氧化硫有毒不能直接排空,用碱液吸收SO2,所以E中盛放液体是碱液,
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若液柱高度保持不变,则气密性良好;D中左侧为短导管,为安全瓶,防止倒吸;装置E起到吸收尾气中SO2、H2S的作用,可选用NaOH溶液,
故答案为:液柱高度保持不变;防止倒吸;NaOH;
(2)装置A中反应的化学方程式为:Na2SO3+H2SO4═Na2SO4+SO2↑+H2O,根据题目所给3个反应,可得出对应关系:2Na2S~2H2S~3S~3Na2SO3,2Na2S反应时同时生成2Na2SO3,还需要1Na2SO3,所以烧瓶C中Na2S和Na2SO3物质的量之比为2:1,
故答案为:2:1;
(3)观察SO2的生成速率,是通过观察溶液中产生气泡的快慢来判断,所以溶液不能与SO2反应,选项中只有饱和NaHSO3溶液与二氧化硫不反应,
故答案为:c;
(4)检测产品中是否存在Na2SO4,操作、现象和结论为取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质,
故答案为:取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质.
| ||
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若液柱高度保持不变,则气密性良好;D中左侧为短导管,为安全瓶,防止倒吸;装置E起到吸收尾气中SO2、H2S的作用,可选用NaOH溶液,
故答案为:液柱高度保持不变;防止倒吸;NaOH;
(2)装置A中反应的化学方程式为:Na2SO3+H2SO4═Na2SO4+SO2↑+H2O,根据题目所给3个反应,可得出对应关系:2Na2S~2H2S~3S~3Na2SO3,2Na2S反应时同时生成2Na2SO3,还需要1Na2SO3,所以烧瓶C中Na2S和Na2SO3物质的量之比为2:1,
故答案为:2:1;
(3)观察SO2的生成速率,是通过观察溶液中产生气泡的快慢来判断,所以溶液不能与SO2反应,选项中只有饱和NaHSO3溶液与二氧化硫不反应,
故答案为:c;
(4)检测产品中是否存在Na2SO4,操作、现象和结论为取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质,
故答案为:取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质.
看了工业上常利用含硫废水生产Na2...的网友还看了以下:
1、-0.2(5x^2+1)2、-3(2x-1)+7X3、-3(2x-2/3Y^2)+2(-3/2 2020-05-16 …
3-x5-----÷(x+2----------)其中x=2√2,先化简,再求值.(中间的横线是分 2020-06-07 …
盒中有6只灯泡,其中2只次品,4只正品,有放回地从中任取两次,每次取一只,试求下列事件的概率:(1 2020-06-13 …
再再续化学题在120C°时分别进行以下四个反应:1.2H2s(s)+O2(g)===2H2O(g) 2020-07-09 …
ax^2-1/9ab^2-ab-2a^2b-a^3b3a^2bc^3+6ac^2-9acdx^n+ 2020-07-22 …
求个正则表达式,Java能用的字符串为1+2+3+4这种类型其中1234为数字+可以是+-*/中的 2020-07-23 …
解不等式log2(2x-1)∙log(1/2)(2^(x+1)-2)>-2其中2,1/2是底数(2 2020-07-30 …
椭圆的范围对于椭圆的标准方程y^2/b^2+x^2/a^2=1中为什么y^2/b^2=1-(x^2 2020-08-02 …
算一算.42÷2=44÷2=4中÷2=4z÷2=的0÷2=中地÷地=中中÷地=中9÷地=72÷地=的 2020-10-31 …
一个口袋中有红球3个,白球4个.(Ⅰ)从中不放回地摸球,每次摸2个,摸到的2个球中至少有1个红球则中 2020-11-04 …