早教吧作业答案频道 -->化学-->
现有反应:A.CaCO3═CaO+CO2B.Zn+H2SO4═ZnSO4+H2C.C+CO2═2COD.2KOH+H2SO4═K2SO4+2H2O(1)上述四个反应中属于氧化还原反应且反应过程中能量变化符合图甲的是(填反应序号).(2)在常温
题目详情
现有反应:A.CaCO3═CaO+CO2
B.Zn+H2SO4═ZnSO4+H2
C.C+CO2═2CO
D.2KOH+H2SO4═K2SO4+2H2O
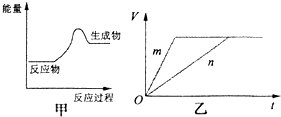
(1)上述四个反应中属于氧化还原反应且反应过程中能量变化符合图甲的是___(填反应序号).
(2)在常温下,上述四个反应中可用于设计原电池的是___(填反应序号),根据该原电池回答下列问题:
①负极材料是___,负极发生___(填“氧化”或“还原”)反应;正极反应式为___.
②当导线中有1mol电子通过时,理论上发生的变化是___(填序号).
a.溶液增重32.5g b.溶液增重31.5g c.析出1gH2 d.析出11.2LH2
(3)对于反应B,将足量且等量的形状相同的锌块分别加入到等浓度等体积的两份稀硫酸X、Y中,同时向X中加入少量饱和CuSO4溶液,发生反应生成氢气的体积(V)与时间(t)的关系如图乙所示.
①m曲线表示锌与稀硫酸___(填“X”或“Y”)反应.
②锌分别与稀硫酸X、Y反应时,反应速率不同的原因是___(填序号).
a.CuSO4作催化剂
b.加入硫酸铜溶液增大了c(SO
)
c.Zn首先与Cu2+反应,生成的Cu与Zn、稀硫酸构成原电池
d.加入硫酸铜溶液增大了溶液体积.
B.Zn+H2SO4═ZnSO4+H2
C.C+CO2═2CO
D.2KOH+H2SO4═K2SO4+2H2O

(1)上述四个反应中属于氧化还原反应且反应过程中能量变化符合图甲的是___(填反应序号).
(2)在常温下,上述四个反应中可用于设计原电池的是___(填反应序号),根据该原电池回答下列问题:
①负极材料是___,负极发生___(填“氧化”或“还原”)反应;正极反应式为___.
②当导线中有1mol电子通过时,理论上发生的变化是___(填序号).
a.溶液增重32.5g b.溶液增重31.5g c.析出1gH2 d.析出11.2LH2
(3)对于反应B,将足量且等量的形状相同的锌块分别加入到等浓度等体积的两份稀硫酸X、Y中,同时向X中加入少量饱和CuSO4溶液,发生反应生成氢气的体积(V)与时间(t)的关系如图乙所示.
①m曲线表示锌与稀硫酸___(填“X”或“Y”)反应.
②锌分别与稀硫酸X、Y反应时,反应速率不同的原因是___(填序号).
a.CuSO4作催化剂
b.加入硫酸铜溶液增大了c(SO
| 2- 4 |
c.Zn首先与Cu2+反应,生成的Cu与Zn、稀硫酸构成原电池
d.加入硫酸铜溶液增大了溶液体积.
▼优质解答
答案和解析
(1)图1中反应物的总能量低于生成物的总能量,此图表示的反应为吸热反应,
A、CaCO3
CaO+CO2↑,没有化合价的变化,不是氧化还原反应,故A错误;
B、Zn+H2SO4═ZnSO4+H2↑,金属与酸的反应为放热反应,故B错误;
C、C+CO2
2CO,此反应中C的化合价升高,二氧化碳中C元素化合价降低,属于氧化还原反应且为吸热反应,故C正确;
D、2KOH+H2SO4═K2SO4+2H2O,此反应为复分解反应,不属于氧化还原反应,故D错误;
故选C;
(2)B和C均为氧化还原反应,但是C不能在常温下进行,锌与稀硫酸的反应为自发的氧化还原反应,能被设计成原电池,
故答案为:B;
①Zn易失电子作负极,电极反应式为Zn-2e-=Zn2+,发生氧化反应,Cu或石墨作正极,正极上电极反应式为2H++2e-=H2↑,
故答案为:Zn;氧化;2H++2e-=H2↑;
②导线中有1mol电子通过时,Zn-2e-=Zn2+,负极锌物质的量减小0.5mol,质量减小0.5mol×65g/mol=32.5g;铜片(或石墨)上放出氢气,2H++2e-=H2↑,根据电子守恒生成氢气的物质的量0.5mol,质量为0.5mol×2g/mol=1g,故溶液增重32.5-1=31.5g,因为未说明气体所处的稳度与压强,故d错误,所以选项中bc正确,
故答案为:bc;
(3)①由图2可知,反应m反应速率比反应n快,m曲线表示锌与稀硫酸中加入少量饱和CuSO4溶液的反应,原电池加快反应速率,
故答案为:X;
②由于锌是足量的,稀硫酸的物质的量相同,则产生氢气的质量相同,由于X中加入少量硫酸铜溶液,锌置换出少量的Cu,与Zn和稀硫酸构成原电池,加快反应速率,
故答案为c.
A、CaCO3
| ||
B、Zn+H2SO4═ZnSO4+H2↑,金属与酸的反应为放热反应,故B错误;
C、C+CO2
| ||
D、2KOH+H2SO4═K2SO4+2H2O,此反应为复分解反应,不属于氧化还原反应,故D错误;
故选C;
(2)B和C均为氧化还原反应,但是C不能在常温下进行,锌与稀硫酸的反应为自发的氧化还原反应,能被设计成原电池,
故答案为:B;
①Zn易失电子作负极,电极反应式为Zn-2e-=Zn2+,发生氧化反应,Cu或石墨作正极,正极上电极反应式为2H++2e-=H2↑,
故答案为:Zn;氧化;2H++2e-=H2↑;
②导线中有1mol电子通过时,Zn-2e-=Zn2+,负极锌物质的量减小0.5mol,质量减小0.5mol×65g/mol=32.5g;铜片(或石墨)上放出氢气,2H++2e-=H2↑,根据电子守恒生成氢气的物质的量0.5mol,质量为0.5mol×2g/mol=1g,故溶液增重32.5-1=31.5g,因为未说明气体所处的稳度与压强,故d错误,所以选项中bc正确,
故答案为:bc;
(3)①由图2可知,反应m反应速率比反应n快,m曲线表示锌与稀硫酸中加入少量饱和CuSO4溶液的反应,原电池加快反应速率,
故答案为:X;
②由于锌是足量的,稀硫酸的物质的量相同,则产生氢气的质量相同,由于X中加入少量硫酸铜溶液,锌置换出少量的Cu,与Zn和稀硫酸构成原电池,加快反应速率,
故答案为c.
看了现有反应:A.CaCO3═Ca...的网友还看了以下:
3句英译汉1.Idon'tbelieveyou'resorry.2.Thatwasclumsyof 2020-04-06 …
关于Cl[2]O的一道题Cl[2]O常用NaClO[3]和Na[2]SO[3]溶液混合并加H[2] 2020-04-11 …
初三数学一元二次方程题1.探索下列方程的解(写出探索过程):(1)x^2-5x+6=0;(2)2x 2020-05-14 …
已知A(3.0),B(0.3),C(cosa.sina) 1.若向量AC×向量BC=-1,求sin 2020-05-16 …
(1+1/2+1/3+1/5)*(1/2+1/3+1/5+1/7)-(1+1/2+1/3+1/5+ 2020-06-08 …
能同时被2、3整除的最小三位数是能同时被3、5整除的最小三位数是能同时被2、3、5整除的最小三位数 2020-06-11 …
50ax^2-98ay^254x^2y^2-36x^2y=6x^22a^2b^2-10a^2b-1 2020-07-19 …
一列数按“3,0,2,1,3,O,2,1,3,O,2,丨,……”排列,问:第36个数是几?这36个 2020-07-19 …
数学的贝克莱悖论如何解决的?当x增长为x+o时,x的立方(记为x^3)成为(x+o)的立方(记为( 2020-07-24 …
在平面直角坐标系中,将点P(2,3)绕原点O顺时针旋转90°后得到点P′,则点P′的坐标是()A.( 2020-12-25 …