早教吧作业答案频道 -->化学-->
某工厂对工业生产钛白粉产生的废液进行综合利用,废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,可用于生产颜料铁红和补血剂乳酸亚铁.其生产工艺流程如下:已知:①TiOSO4可溶于
题目详情
某工厂对工业生产钛白粉产生的废液进行综合利用,废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,可用于生产颜料铁红和补血剂乳酸亚铁.其生产工艺流程如下:
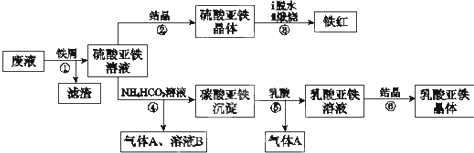
已知:①TiOSO4可溶于水,在水中可以电离为TiO2+和SO42-;
②TiOSO4水解的反应为:TiOSO4+(x+1)H2O→TiO2•xH2O↓+H2SO4.
请回答:
(1)步骤①所得滤渣的主要成分为___,分离硫酸亚铁溶液和滤渣的操作中所用的玻璃仪器是___;步骤②中得到硫酸亚铁晶体的操作为蒸发浓缩、___.
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为___.
(3)步骤④的离子方程式是___.
(4)已知:FeCO3(S)⇌Fe2+(aq)+CO32-(aq),试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因___.
(5)实验室中常用KMnO4滴定法测定晶体中FeSO4•7H2O的质量分数,取步骤②中所得FeSO4•7H2O晶体样品a g,配成500.00mL溶液,取出25.00mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应).若消耗0.1000mol•L-1 KMnO4溶液25.00mL,所得晶体中FeSO4•7H2O的质量分数为(用a表示)___.

已知:①TiOSO4可溶于水,在水中可以电离为TiO2+和SO42-;
②TiOSO4水解的反应为:TiOSO4+(x+1)H2O→TiO2•xH2O↓+H2SO4.
请回答:
(1)步骤①所得滤渣的主要成分为___,分离硫酸亚铁溶液和滤渣的操作中所用的玻璃仪器是___;步骤②中得到硫酸亚铁晶体的操作为蒸发浓缩、___.
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为___.
(3)步骤④的离子方程式是___.
(4)已知:FeCO3(S)⇌Fe2+(aq)+CO32-(aq),试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因___.
(5)实验室中常用KMnO4滴定法测定晶体中FeSO4•7H2O的质量分数,取步骤②中所得FeSO4•7H2O晶体样品a g,配成500.00mL溶液,取出25.00mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应).若消耗0.1000mol•L-1 KMnO4溶液25.00mL,所得晶体中FeSO4•7H2O的质量分数为(用a表示)___.
▼优质解答
答案和解析
废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,加铁屑,Fe与H2SO4和少量Fe2(SO4)3反应生成FeSO4,TiOSO4水解生成TiO2•xH2O,过滤,滤渣为TiO2•xH2O、Fe,滤液为FeSO4,FeSO4溶液通过蒸发浓缩、冷却结晶...
看了某工厂对工业生产钛白粉产生的废...的网友还看了以下:
在工业生产中把分析纯36%的盐酸稀释成4%的盐酸1200L,需要浓盐酸多少升?第一种算法:4%*1 2020-05-16 …
写化学方程式1.硫酸跟氧化镁反应,生成硫酸镁和水.2.硫酸跟氢氧化钠溶液反应.生成硫酸钠和水.3. 2020-05-17 …
平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质).某 2020-07-15 …
眼用凝胶的用法曾经治疗情况和效果:在9月4日已去过天津眼科医院,让用硫酸阿托品眼用凝胶滴眼想得到怎样 2020-11-21 …
醋酸钠溶液水解pH计算0.1M的醋酸钠溶液,已知醋酸电离pka=4.76.醋酸钠溶液暴露空气中接触了 2020-12-31 …
常温下有下列四种溶液:①②③④溶液pH=4的NH4ClpH=4的盐酸0.1mol•L-1的醋酸0.1 2021-02-01 …
常温下有下列四种溶液:①②③④溶液pH=4的NH4ClpH=4的盐酸0.1mol•L-1的醋酸0.1 2021-02-01 …
加热27·4克碳酸钠和碳酸氢钠的混合物,直到不再产生气体为止,若标况下生成4.48升的气体问原碳酸钠 2021-02-09 …
已知铜单质与稀硝酸会发生反应,化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H 2021-02-13 …
7.68g铜和一定量的硝酸反应,当铜全部溶解,若生成气体4.48L(已折算成标准状况),求参加反应的 2021-02-17 …