早教吧作业答案频道 -->化学-->
工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)CH3COOC2H5(l)+H2O(l)ΔH=-8.62kJ·mol-1已知CH3COOH、C2H5OH和CH3COOC2H5的沸点依次为118℃、78℃和77℃
题目详情
工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:
CH 3 COOH(l)+C 2 H 5 OH(l) CH 3 COOC 2 H 5 (l)+H 2 O(l) ΔH=-8.62kJ·mol -1
CH 3 COOC 2 H 5 (l)+H 2 O(l) ΔH=-8.62kJ·mol -1
已知CH 3 COOH、C 2 H 5 OH和CH 3 COOC 2 H 5 的沸点依次为118℃、78℃和77℃。在其他条件相同时,某研究小组进行了多次实验,实验结果如图所示。
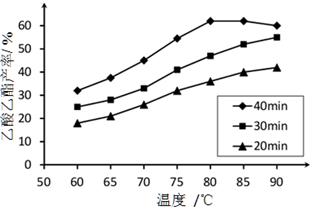
(1)该研究小组的实验目的是__________________。
(2)60℃下反应40min与70℃下反应20min相比,前者的平均反应速率___________后者(填“小于”、“等于”或“大于”)。
(3)如图所示,反应时间为40min、温度超过80℃时,乙酸乙酯产率下降的原因可能是______(写出两条)。
(4)某温度下,将0.10 mol CH 3 COOH溶于水配成1 L溶液。
①实验测得已电离的醋酸分子占原有醋酸分子总数的1.3%,则该温度下CH 3 COOH的电离平衡常数K=____________________。(水的电离忽略不计,醋酸电离对醋酸分子浓度的影响忽略不计)
②向该溶液中再加入__________mol CH 3 COONa可使溶液的pH约为4。(溶液体积变化忽略不计)
CH 3 COOH(l)+C 2 H 5 OH(l)
 CH 3 COOC 2 H 5 (l)+H 2 O(l) ΔH=-8.62kJ·mol -1
CH 3 COOC 2 H 5 (l)+H 2 O(l) ΔH=-8.62kJ·mol -1 已知CH 3 COOH、C 2 H 5 OH和CH 3 COOC 2 H 5 的沸点依次为118℃、78℃和77℃。在其他条件相同时,某研究小组进行了多次实验,实验结果如图所示。

(1)该研究小组的实验目的是__________________。
(2)60℃下反应40min与70℃下反应20min相比,前者的平均反应速率___________后者(填“小于”、“等于”或“大于”)。
(3)如图所示,反应时间为40min、温度超过80℃时,乙酸乙酯产率下降的原因可能是______(写出两条)。
(4)某温度下,将0.10 mol CH 3 COOH溶于水配成1 L溶液。
①实验测得已电离的醋酸分子占原有醋酸分子总数的1.3%,则该温度下CH 3 COOH的电离平衡常数K=____________________。(水的电离忽略不计,醋酸电离对醋酸分子浓度的影响忽略不计)
②向该溶液中再加入__________mol CH 3 COONa可使溶液的pH约为4。(溶液体积变化忽略不计)
▼优质解答
答案和解析
分 析:
(1)根据图中信息可以得出此实验的目的是探究反应温度、反应时间对乙酸乙酯产率的影响。
(2)温度越高,反应速率越大,故前者的平均反应速率小于后者。
(3)ΔH=-8.62kJ·mol -1 ,即反应为放热反应,达到平衡时化学反应逆向移动。故乙酸乙酯产率下降的原因可能是反应可能已达平衡状态,温度升高平衡向逆反应方向移动;温度过高,乙醇和乙酸大量挥发使反应物利用率下降。
(4)①经过公式计算得: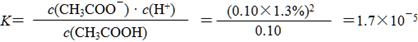 。
。
点评:
本题考查的是化学反应速率的影响因素、化学平衡移动和电离平衡常数计算的知识,题目难度较大,考查学生对基础知识的掌握和计算的能力。
(10分)
(1)探究反应温度、反应时间对乙酸乙酯产率的影响 (2分)
(自变量、因变量有遗漏或表达不清,扣1分)
(2)小于(2分)(“<”得1分)
(3)反应可能已达平衡状态,温度升高平衡向逆反应方向移动;温度过高,乙醇和乙酸大量挥发使反应物利用率下降(2分)
(4)①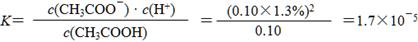 (2分)
(2分)
(因计算时未作近似处理使小数在1.69~1.71之间均不扣分)
②1.7×10 -2 (2分)
(“1.69×10 -2 ~1.71×10 -2 ”或用小数表示均不扣分)
(1)探究反应温度、反应时间对乙酸乙酯产率的影响 (2分)
(自变量、因变量有遗漏或表达不清,扣1分)
(2)小于(2分)(“<”得1分)
(3)反应可能已达平衡状态,温度升高平衡向逆反应方向移动;温度过高,乙醇和乙酸大量挥发使反应物利用率下降(2分)
(4)①
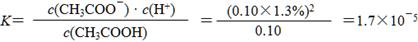 (2分)
(2分)(因计算时未作近似处理使小数在1.69~1.71之间均不扣分)
②1.7×10 -2 (2分)
(“1.69×10 -2 ~1.71×10 -2 ”或用小数表示均不扣分)
分 析:
(1)根据图中信息可以得出此实验的目的是探究反应温度、反应时间对乙酸乙酯产率的影响。
(2)温度越高,反应速率越大,故前者的平均反应速率小于后者。
(3)ΔH=-8.62kJ·mol -1 ,即反应为放热反应,达到平衡时化学反应逆向移动。故乙酸乙酯产率下降的原因可能是反应可能已达平衡状态,温度升高平衡向逆反应方向移动;温度过高,乙醇和乙酸大量挥发使反应物利用率下降。
(4)①经过公式计算得:
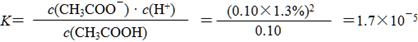 。
。点评:
本题考查的是化学反应速率的影响因素、化学平衡移动和电离平衡常数计算的知识,题目难度较大,考查学生对基础知识的掌握和计算的能力。
看了工业上常利用醋酸和乙醇合成有机...的网友还看了以下:
有20个数第一个数是9以后每个数都比前一个数大3这20个数的和是多少有20个数,第一个数是9,以后 2020-05-15 …
O(∩_∩)O哈哈~O(∩_∩)O~(*^__^*)嘻嘻……那个可爱哦?对了撒~大家有一些可爱的网 2020-05-17 …
∵EM是⊙O的切线,怎么推出EB•EC=EM2①?,看题后回答.(2005•温州)如图,已知四边形 2020-05-21 …
盈不足术怎么算(⊙o⊙)?有人在林中散步,无意中听到几个强盗在商量怎样分配抢来的布匹。若每人分6匹 2020-06-15 …
猜字谜:第一句:我有一物生的巧,半边鳞甲半边毛,半边离水难活命,半边入水命难保.第二句:我有一物分 2020-06-20 …
做物理题时,有些概念一直混淆不清,老师让我好好看看书,可是我不知道要看什么,课本上有概念,可是我不 2020-06-21 …
某药物A是一种具有止血、镇咳、祛痰的芳香烃的衍生物,是阿司匹林的同分异构体,它具有如图转化关系:下 2020-06-23 …
1、桌面上有7个相同的杯子,杯口都朝上,现在每次翻转5个杯子,请问翻转多少次后所有的杯子杯口都朝下 2020-06-27 …
大气臭氧层的反应是:O+O3=2O2△H,该反应的能量变化如图所示,下列叙述中,正确的是()A.O+ 2020-10-31 …
已知正方形ABCD的对角线AC、BD交于O,点O是正方形EFGO的一个顶点,若正方形ABCD的边长为 2020-11-10 …