早教吧作业答案频道 -->化学-->
乙醇的沸点是78℃,能与水以任意比混溶,易与氯化钙结合生成配合物.乙醚的沸点为34,.6℃,难溶于水,乙醚极易燃烧.实验室制乙醚的反应原理是2CH3CH2OH浓H2SO4
题目详情
乙醇的沸点是78℃,能与水以任意比混溶,易与氯化钙结合生成配合物.乙醚的沸点为34,.6℃,难溶于水,乙醚极易燃烧.实验室制乙醚的反应原理是2CH3CH2OH
CH3CH2-O-CH2CH3(乙醚)+H2O
实验步骤:
Ⅰ.乙醚的制备
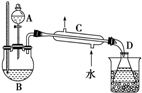
在分液漏斗中加入2mL 95%的乙醇,在一干燥的三颈烧瓶中放入12mL 95%的乙醇,在冷水浴中的冷却下边摇动边缓慢加入12mL浓硫酸,使混合均匀,并加入2粒沸石.实验装置如图:将反应瓶放在电热套上加热,使温度迅速地上升到140℃,开始由分液漏斗慢慢滴加乙醇,控制流速并保持温度在135~140℃之间.待乙醇加完后,继续反应10min,直到温度上升到160℃止.关闭热源,停止反应.
Ⅱ.乙醚的精制
将馏出物倒入分液漏斗中,依次用8mL 15% NaOH溶液、8mL饱和食盐水洗涤,最后再用8mL饱和氯化钙溶液洗涤2次,充分静置后分液.将乙醚倒入干燥的锥形瓶中,用块状无水氯化钙干燥.待乙醚干燥后,加入到蒸馏装置中用热水浴蒸馏,收集33~38℃的馏分.
请根据上述信息,完成下列问题:
(1)乙醚的制备和精制过程中都需要使用沸石,其作用是___,如果实验中忘记加沸石,需要怎么处理?___.
(2)乙醚的制备和精制过程中都需要使用温度计,其水银球位置是否相同?___(填“是”或“否”),原因是___
(3)仪器C的名称为___.
(4)如果温度太高,将会发生副反应,产物是___.
(5)精制乙醚中,加入15% NaOH溶液的作用是___,加入饱和氯化钙溶液的作用是___.
| 浓H2SO4 |
| |
| 140℃ |
实验步骤:
Ⅰ.乙醚的制备
在分液漏斗中加入2mL 95%的乙醇,在一干燥的三颈烧瓶中放入12mL 95%的乙醇,在冷水浴中的冷却下边摇动边缓慢加入12mL浓硫酸,使混合均匀,并加入2粒沸石.实验装置如图:将反应瓶放在电热套上加热,使温度迅速地上升到140℃,开始由分液漏斗慢慢滴加乙醇,控制流速并保持温度在135~140℃之间.待乙醇加完后,继续反应10min,直到温度上升到160℃止.关闭热源,停止反应.
Ⅱ.乙醚的精制
将馏出物倒入分液漏斗中,依次用8mL 15% NaOH溶液、8mL饱和食盐水洗涤,最后再用8mL饱和氯化钙溶液洗涤2次,充分静置后分液.将乙醚倒入干燥的锥形瓶中,用块状无水氯化钙干燥.待乙醚干燥后,加入到蒸馏装置中用热水浴蒸馏,收集33~38℃的馏分.
请根据上述信息,完成下列问题:

(1)乙醚的制备和精制过程中都需要使用沸石,其作用是___,如果实验中忘记加沸石,需要怎么处理?___.
(2)乙醚的制备和精制过程中都需要使用温度计,其水银球位置是否相同?___(填“是”或“否”),原因是___
(3)仪器C的名称为___.
(4)如果温度太高,将会发生副反应,产物是___.
(5)精制乙醚中,加入15% NaOH溶液的作用是___,加入饱和氯化钙溶液的作用是___.
▼优质解答
答案和解析
(1)液体加热加沸石,是防止液体瀑沸,如果实验中忘记加沸石,停止加热,冷却后补加,否则也会引起瀑沸,所以乙醚的制备和精制过程中都需要使用沸石,其作用是防止暴沸,如果实验中忘记加沸石,停止加热,冷却后补加,
故答案为:防止暴沸;停止加热,冷却后补加;
(2)乙醚的制备过程中要测量反应溶液的温度,所以水银球位置在溶液中间,而精制过程中需要测量蒸出物的沸点,水银球位置在蒸馏烧瓶的支管处,所以它们的位置不同,
故答案为:否;制备要控制反应液的温度,水银球要放在反应液里;蒸馏要测馏份的温度,要放在支管口处;
(3)根据装置图可知仪器C的名称为冷凝管,
故答案为:(直形)冷凝管;
(4)乙醇在浓硫酸作用下加热到170℃就可以生成乙烯,如果温度太高,将会发生副反应,产物是乙烯,
故答案为:乙烯;
(5)精制乙醚中,馏出物中可能有酸性杂质,馏出物中乙醇,可以用饱和氯化钙溶液除去,精制乙醚中,加入15% NaOH溶液的作用是 除去酸性杂质,加入饱和氯化钙溶液的作用是除乙醇,
故答案为:除去酸性杂质;除乙醇.
故答案为:防止暴沸;停止加热,冷却后补加;
(2)乙醚的制备过程中要测量反应溶液的温度,所以水银球位置在溶液中间,而精制过程中需要测量蒸出物的沸点,水银球位置在蒸馏烧瓶的支管处,所以它们的位置不同,
故答案为:否;制备要控制反应液的温度,水银球要放在反应液里;蒸馏要测馏份的温度,要放在支管口处;
(3)根据装置图可知仪器C的名称为冷凝管,
故答案为:(直形)冷凝管;
(4)乙醇在浓硫酸作用下加热到170℃就可以生成乙烯,如果温度太高,将会发生副反应,产物是乙烯,
故答案为:乙烯;
(5)精制乙醚中,馏出物中可能有酸性杂质,馏出物中乙醇,可以用饱和氯化钙溶液除去,精制乙醚中,加入15% NaOH溶液的作用是 除去酸性杂质,加入饱和氯化钙溶液的作用是除乙醇,
故答案为:除去酸性杂质;除乙醇.
看了乙醇的沸点是78℃,能与水以任...的网友还看了以下:
初2科学应用题甲、乙都是圆柱体,有不同的金属材料制成,起底面积分别为S=20,S=15,高度之比是 2020-04-27 …
(2006•顺义区一模)甲、乙两个长方体,由不同材料制成,其中底面积分别为S甲=40cm2、S乙= 2020-06-04 …
(2006•顺义区一模)甲、乙两个长方体,由不同材料制成,其中底面积分别为S甲=40cm2、S乙= 2020-06-15 …
甲\乙两个长方体由不同的材料制成,其底面积分别为S甲=40CM2,S乙=30CM2,高度之比H甲: 2020-06-15 …
如图所示,甲乙两个均匀圆柱体分别放在水平地面上,它们对地面的压强相等,己知r甲=2r乙,h甲=2r 2020-07-08 …
1、甲、乙两车从A、B两地相向而行,已知甲车速度为60km/h,乙车速度是100km/h,甲车比乙 2020-07-23 …
甲乙两个长方体.由不同材料制成.其地面积分别为S甲=40平方厘米.S乙=30平方厘米.高度之比h甲比 2020-11-17 …
有甲、乙两个光滑的斜面,高度之比h甲:h乙=1:3,长度之比l甲:l乙=3:1,将同一物体分别沿甲、 2020-11-29 …
甲、乙两个形状未知的容器的底面积之比为S甲:S乙=4:3,两容器内盛有同一种液体,如果两容器底面积所 2020-11-29 …
如图所示,甲乙两个均匀圆柱体分别放在水平地面上,它们对地面的压强相等,己知r甲=2r乙,h甲=2r甲 2021-01-12 …