早教吧作业答案频道 -->化学-->
化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题:(1)已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃.室温时AX3与气体X2反应生成lmolAX5,放出热量123.8kJ.
题目详情
化合物AX3和单质X2在一定条件下反应可生成化合物AX5.回答下列问题:
(1)已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃.室温时AX3与气体X2反应生成l mol AX5,放出热量123.8kJ.该反应的热化学方程式为___.
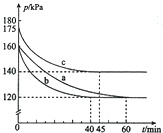
(2)反应AX3(g)+X2(g)⇌AX5(g)在容积为10L的密闭容器中进行.起始时AX3和X2均为0.2mol.反应在不同条件下进行,反应体系总压强随时间的变化如图所示.
①实验a从反应开始至达到平衡时的反应速率 v(AX5)=___;
②图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为___(填实验序号);与实验a相比,其他两组改变的实验条件及判断依据是:b___、c___.
③用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,则α的表达式为___.

(1)已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃.室温时AX3与气体X2反应生成l mol AX5,放出热量123.8kJ.该反应的热化学方程式为___.
(2)反应AX3(g)+X2(g)⇌AX5(g)在容积为10L的密闭容器中进行.起始时AX3和X2均为0.2mol.反应在不同条件下进行,反应体系总压强随时间的变化如图所示.
①实验a从反应开始至达到平衡时的反应速率 v(AX5)=___;
②图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为___(填实验序号);与实验a相比,其他两组改变的实验条件及判断依据是:b___、c___.
③用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,则α的表达式为___.
▼优质解答
答案和解析
(1)因为AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃,室温时,AX3为液态,AX5为固态,生成1mol AX5,放出热量123.8kJ,该反应的热化学方程为:AX3(l)+X2(g)=AX5(s)△H=-123.8kJ•mol-1,
故答案为:AX3(l)+X2(g)=AX5(s)△H=-123.8kJ•mol-1;
(2)①起始时AX3和X2均为0.2mol,即no=0.4mol,总压强为160KPa,平衡时总压强为120KPa,设平衡时总物质的量为n,根据压强之比就等于物质的量之比有:
=
,n=0.30mol,
AX3(l)+X2(g)⇌AX5(g)
初始 (mol) 0.20 0.20 0
平衡 (mol) 0.20-x 0.20-x x
(0.20-x)+(0.20-x)+x=0.30
x=0.10
v( AX5)=
=1.7×10-4mol/(L•min),
故答案为:1.7×10-4mol•L-1•min-1
②根据到abc达平衡用时的多少可以比较出反应速率的大小为:b>c>a;
与实验a相比,b实验到达平衡的时间变小,但平衡没有发生移动,所以为使用催化剂;c实验到达平衡时总压强变大,说明平衡逆向移动,而化学反应速率变大,考虑到该反应是放热反应,所以是升高温度所导致的,
故答案为:bca;加入催化剂,反应速率加快,但平衡点没有改变;温度升高,反应速率加快,但平衡点向逆反应方向移动(或反应容器的容积和起始物质的量未改变,但起始总压强增大);
③用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,根据压强之比就等于物质的量之比有:
,n=
,
AX3(g)+X2(g)⇌AX5(g)
初始 (mol) 0.20 0.20 0
平衡 (mol) 0.20-x 0.20-x x
(0.20-x)+(0.20-x)+x=n
x=0.40-n=0.4-
α=
×100%=2(1-
)×100%,
故答案为:α=2(1-
)×100%;
故答案为:AX3(l)+X2(g)=AX5(s)△H=-123.8kJ•mol-1;
(2)①起始时AX3和X2均为0.2mol,即no=0.4mol,总压强为160KPa,平衡时总压强为120KPa,设平衡时总物质的量为n,根据压强之比就等于物质的量之比有:
| 120Kpa |
| 160KPa |
| n |
| 0.4mol |
AX3(l)+X2(g)⇌AX5(g)
初始 (mol) 0.20 0.20 0
平衡 (mol) 0.20-x 0.20-x x
(0.20-x)+(0.20-x)+x=0.30
x=0.10
v( AX5)=
| 0.10mol |
| 10L×60min |
故答案为:1.7×10-4mol•L-1•min-1
②根据到abc达平衡用时的多少可以比较出反应速率的大小为:b>c>a;
与实验a相比,b实验到达平衡的时间变小,但平衡没有发生移动,所以为使用催化剂;c实验到达平衡时总压强变大,说明平衡逆向移动,而化学反应速率变大,考虑到该反应是放热反应,所以是升高温度所导致的,
故答案为:bca;加入催化剂,反应速率加快,但平衡点没有改变;温度升高,反应速率加快,但平衡点向逆反应方向移动(或反应容器的容积和起始物质的量未改变,但起始总压强增大);
③用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,根据压强之比就等于物质的量之比有:
| Po |
| P |
| 0.4P |
| Po |
AX3(g)+X2(g)⇌AX5(g)
初始 (mol) 0.20 0.20 0
平衡 (mol) 0.20-x 0.20-x x
(0.20-x)+(0.20-x)+x=n
x=0.40-n=0.4-
| 0.4P |
| Po |
α=
0.4-
| ||
| 0.2 |
| P |
| Po |
故答案为:α=2(1-
| P |
| Po |
看了 化合物AX3和单质X2在一定...的网友还看了以下:
关于数学集合的几个问题1.A=﹛x|x²-mx+3=0﹜,B=﹛x|2x-6=0﹜,⑴若A=空集,求 2020-03-31 …
在短周期中的X和Y两种元素可组成化合物XY3,说法正确的是()A.X和Y一定不属于同一主族B.X和 2020-04-08 …
(1)已知满足方程组3X+5Y=M+22X+3Y=M的X,Y值的和等于2,求M的平方-2M+1的值 2020-04-26 …
若A={x丨x²-mx+m-1=0},B={x丨x²-(2m-1)x+2m=0},且A∩B≠φ,求 2020-05-13 …
若A={x|x^2-mx+m-1=0},B={x|x^2-(2m-1)x+2m=0},且A交上B不 2020-05-13 …
如图,直线y=x+m和抛物线y=ax^2+bx+c都经过点A(1,0),B(3,2).(1)求m的 2020-05-16 …
1、已知关于x的一元二次方程x²-mx-2=0(1)若x=-1是方程的一个根,求m的值和方程的另一 2020-05-16 …
若关于x的方程x^2+(m^2-9)x+m-1=0的两个实数根互为相反数,求m的值和方程的根.若关 2020-05-19 …
已知A={x|x^2-mx+m-1=0},B={x|x^2-(2m-1)x+2m=0}A交B≠空集 2020-05-23 …
已知关于x的方程2分之6m+3x=6的解是关于x的方程(完整题目见问题补充)已知关于x的方程2分之 2020-06-03 …