早教吧作业答案频道 -->化学-->
硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如图所示:已知:①SO2(g)+Cl2(g)催化剂SO2Cl2(l)△H=-97.3kJ•mol-1②硫酰氯
题目详情
硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如图所示:
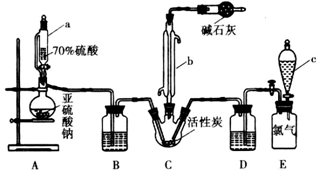
已知:
①SO2(g)+Cl2(g)
SO2Cl2(l)△H=-97.3kJ•mol-1
②硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中易“发烟”;
③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气.
(1)仪器a为恒压分液漏斗,与普通分液漏斗相比,其优点是___.
(2)仪器b的名称为___,干燥管中碱石灰的主要作用是___.
(3)装置E为储气装置,用于提供氯气,则分液漏斗c中盛放的试剂为___.当装置E中排出氯气1.12L(已折算成标准状况)时,最终得到5.4g纯净的硫酰氯,则硫酰氯的产率为___.长期存放的硫酰氯会发黄,其原因可能为___.
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为___,分离这两种液态产物的方法是___.
(5)若将SO2、Cl2按照一定比例通入水中,请设计简单实验验证二者是否恰好完全反应.___(简要描述实验步骤、现象和结论).

已知:
①SO2(g)+Cl2(g)
| 催化剂 |
| |
②硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中易“发烟”;
③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气.
(1)仪器a为恒压分液漏斗,与普通分液漏斗相比,其优点是___.
(2)仪器b的名称为___,干燥管中碱石灰的主要作用是___.
(3)装置E为储气装置,用于提供氯气,则分液漏斗c中盛放的试剂为___.当装置E中排出氯气1.12L(已折算成标准状况)时,最终得到5.4g纯净的硫酰氯,则硫酰氯的产率为___.长期存放的硫酰氯会发黄,其原因可能为___.
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为___,分离这两种液态产物的方法是___.
(5)若将SO2、Cl2按照一定比例通入水中,请设计简单实验验证二者是否恰好完全反应.___(简要描述实验步骤、现象和结论).
▼优质解答
答案和解析
(1)仪器a为恒压分液漏斗,可以平衡分液漏斗内外气压,便于液体顺利流下;
故答案为:平衡分液漏斗内外压强,便于液体顺利流下;
(2)由仪器b的结构特征,可知b为直形冷凝管;装置C中产生硫酰氯,硫酰氯在潮湿空气中“发烟”,所以要用碱石灰防止空气中的水分进入装置C;
故答案为:直形冷凝管(或冷凝管);防止空气中的水分进入装置;
(3)利用分液漏斗中的液体将装置E的氯气排出,与二氧化硫在装置C中反应,分液漏斗可以为饱和食盐水;氯气的物质的量为11.2L÷22.4L/mol═0.05mol,由方程式可知n(SO2Cl2)=n(Cl2)=0.05mol,故理论上生成SO2Cl2的质量为0.05mol×135g/mol=6.75g,故其产率为
×100%=80%;硫酰氯中溶有其分解产生的氯气使长期存放的硫酰氯会发黄;
故答案为:饱和食盐水;80%;硫酰氯中溶有其分解产生的氯气;
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质应为H2SO4,反应的化学方程式为2ClSO3H
SO2Cl2+H2SO4,二者为互溶液体,沸点相差较大,采取蒸馏法进行分离,
故答案为:2ClSO3H
SO2Cl2+H2SO4;蒸馏;
(5)二氧化硫溶液与氯水都可以漂白品红溶液,若二者恰好完全反应得到盐酸、硫酸,不能使品红溶液褪色,检验方案为:取少量反应后的溶液于试管中,滴加品红溶液震荡,若溶液褪色,则二者未完全反应;若不褪色,则二者恰好完全反应;
故答案为:取少量反应后的溶液于试管中,滴加品红溶液震荡,若溶液褪色,则二者未完全反应;若不褪色,则二者恰好完全反应.
故答案为:平衡分液漏斗内外压强,便于液体顺利流下;
(2)由仪器b的结构特征,可知b为直形冷凝管;装置C中产生硫酰氯,硫酰氯在潮湿空气中“发烟”,所以要用碱石灰防止空气中的水分进入装置C;
故答案为:直形冷凝管(或冷凝管);防止空气中的水分进入装置;
(3)利用分液漏斗中的液体将装置E的氯气排出,与二氧化硫在装置C中反应,分液漏斗可以为饱和食盐水;氯气的物质的量为11.2L÷22.4L/mol═0.05mol,由方程式可知n(SO2Cl2)=n(Cl2)=0.05mol,故理论上生成SO2Cl2的质量为0.05mol×135g/mol=6.75g,故其产率为
| 5.4g |
| 6.75g |
故答案为:饱和食盐水;80%;硫酰氯中溶有其分解产生的氯气;
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质应为H2SO4,反应的化学方程式为2ClSO3H
| ||
故答案为:2ClSO3H
| ||
(5)二氧化硫溶液与氯水都可以漂白品红溶液,若二者恰好完全反应得到盐酸、硫酸,不能使品红溶液褪色,检验方案为:取少量反应后的溶液于试管中,滴加品红溶液震荡,若溶液褪色,则二者未完全反应;若不褪色,则二者恰好完全反应;
故答案为:取少量反应后的溶液于试管中,滴加品红溶液震荡,若溶液褪色,则二者未完全反应;若不褪色,则二者恰好完全反应.
看了硫酰氯(SO2Cl2)是一种重...的网友还看了以下:
PCl5的分解反应为:PCl5(g)=PCl3(g)+Cl2(g)在523K时,Kθ=1.85PC 2020-04-07 …
N、C、S元素的单质及化合物在工农业生成中有着重要的应用Ⅰ、CO与Cl2在催化剂的作用下合成光气( 2020-04-11 …
(2012•河北模拟)在体积恒定的密闭容器中,1molA(g)与1molB(g)在催化剂作用下加热 2020-04-11 …
反应CO(g)+Cl2(g)→COCl2(g),经实验测得其速率方程式为r=k[Cl2]n[CO] 2020-05-24 …
下面三个方法都可以用来制氯气:①4HCl(浓)+MnO2△.MnCl2+Cl2↑+2H2O②4HC 2020-07-22 …
CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光 2020-11-30 …
光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合 2020-12-25 …
光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合 2020-12-25 …
在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:PCl3(g) 2021-01-13 …
磺酰氯(SO2Cl2)和亚硫酰氯(SOCl2)均是实验室常见试剂。已知:SO2Cl2(g)SO2(g 2021-02-01 …