在元素周期表中,铝在硼的正下方,它们有很多相似的化学性质,可以形成许多组成和性质类似的化合物。单质硼可以通过硼镁矿Mg2B2O5·H2O来制取。(1)写出步骤①的化学方程
在元素周期表中,铝在硼的正下方,它们有很多相似的化学性质,可以形成许多组成和性质类似的化合物。单质硼可以通过硼镁矿Mg 2 B 2 O 5 ·H 2 O来制取。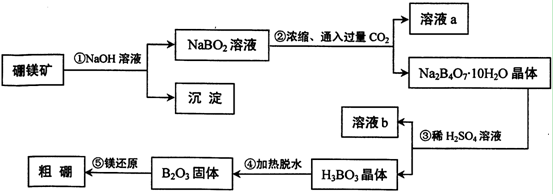
(1)写出步骤①的化学方程式 ,
(2)写出步骤②的离子方程式 ,
(3)写出表示溶液a物料守恒的关系 ;
(4)步骤③中加入稀H 2 SO 4 的作用是 ;
(5)将制得的粗硼在一定条件下反应全部生成BI 3 ,BI 3 热分解可以得到纯净的单质硼。0.25 g粗硼制成的BI 3 分解得到的I 2 全部被收集后,用2.00 mol/L Na 2 S 2 O 3 溶液滴定,达到滴定终点时消耗27.00 mL Na 2 S 2 O 3 溶液。(已知:I 2 +2S 2 O 3 2 - 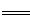 2I - +S 4 O 6 2 - )
2I - +S 4 O 6 2 - )
①滴定过程中所用的指示剂为 ,滴定终点的现象是 ;
②粗硼中硼的含量为____ ;
(6)利用硼砂晶体(Na 2 B 4 O 7 ?10H 2 O)可制备过硼酸钠,它是一种优良的漂白剂,被广泛应用于洗衣粉、漂白粉、洗涤剂中。已知纯净的过硼酸钠晶体中各元素的物质的量之比为以n(Na):n(B):n(H):n(O)=1:1:n:7。取过硼酸钠晶体在70℃以上加热将逐步失去结晶水,测得固体质量随温度的变化如图所示,则乃时所得晶体的化学式为 ,请写出简要的解题过程。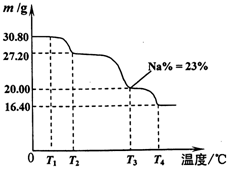
分 析:
(3)通入过量二氧化碳得到的是碳酸氢钠溶液,所以有c(Na+) = c(CO32-) + c(HCO3-) + c(H2CO3) 。(5)①Na2S2O3溶液成碱性,S2O32-离子水解溶液显示碱性,反应的离子方程式为:S2O32-+H2O?HS2O3-+OH-;滴定过程中有碘单质参与,可以使用淀粉溶液作为指示剂;滴定结束时,锥形瓶中溶液蓝色褪去且30s内不褪色。②硫代硫酸钠的物质的量为:2.00mol/L×0.027L=0.054mol,根据关系式:B~BI3~3/2I2~3S2O32-,n(B)=1/3n(S2O32-)=0.018mol,硼的质量为:11g/mol×0.018mol=0.1944g,粗硼中硼的含量为:×100%=79.2%,故答案为:79.2%;
考点:
考查本题考查了盐类的水解、复杂化学式的计算等。
不用化学方法进行鉴别,通过的实验事实证明Na2O2已变质,变质的过程中发生的三个化学方程式是(不考 2020-05-13 …
某优良品种水稻的基因型为AaBb,其花药通过组织培养形成了试管苗.下列对这一培养过程的叙述,错误的 2020-06-06 …
关于化学方程式、专家解答232、在偏铝酸钠中通入少量氯化氢气体(反应的化学方程式和离子方程式)33 2020-07-17 …
参数方程化简问题形如x=1/(k^2)+k^2y=1/k+k的参数方程如何化简成普通方程 2020-08-01 …
给出下列说法:①圆的渐开线的参数方程不能转化为普通方程;②圆的渐开线也可以转化为普通方程,但是转化 2020-08-01 …
给出下列说法①圆的渐开线的参数方程不能转化为普通方程;②圆的渐开线也可以转化为普通方程但是转化后的 2020-08-01 …
x=t+1/t,y=t-1/t化成普通方程x=t+1/t,y=t-1/t(t为参数),化成x=t+ 2020-08-02 …
将参数方程化为普通方程x=t-sinty=1-cost将参数方程化为普通方程x=t-sinty=1 2020-08-02 …
下列关于生物进化证据的说法中,正确的是()A.通过细胞色素C的研究可以知道生物进化的历程B.同源器官 2020-11-06 …
将下列普通方程化为含t的参数方程1.y^3(2a-x)=x^4--->化为:y=tx的形式2.y(2 2021-02-10 …