早教吧作业答案频道 -->化学-->
硅单质及其化合物应用范围很广.制备硅半导体材料必须先得到高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如图1:(1)第①步制备粗硅的化学方程
题目详情
硅单质及其化合物应用范围很广.制备硅半导体材料必须先得到高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如图1:
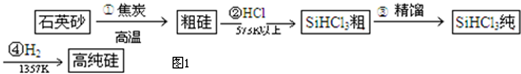
(1)第①步制备粗硅的化学方程式为___.第④步由纯SiHCl3制备高纯硅的化学方程式为___.
(2)用SiHCl3与过量H2反应制备纯硅的装置如图2所示(热源及夹持装置均已略去):
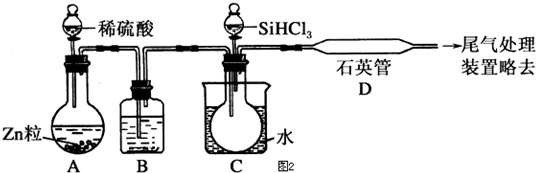
①装置B中的试剂是___,装置C中的烧瓶需要加热,其目的是___.
②反应一段时间后,装置D中观察到的现象是___,装置D不能采用普通玻璃管的原因是___.
③SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式:___;H2还原SiHCl3过程中若混入O2,可能引起的后果是___;整个制备过程必须严格控制___.
(3)下列有关硅材料的说法正确的是___(填字母).
A.碳化硅硬度大,可用于生产砂纸、砂轮等
B.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
C.高纯度的二氧化硅可用于制造高性能通讯材料--光导纤维
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅.

(1)第①步制备粗硅的化学方程式为___.第④步由纯SiHCl3制备高纯硅的化学方程式为___.
(2)用SiHCl3与过量H2反应制备纯硅的装置如图2所示(热源及夹持装置均已略去):

①装置B中的试剂是___,装置C中的烧瓶需要加热,其目的是___.
②反应一段时间后,装置D中观察到的现象是___,装置D不能采用普通玻璃管的原因是___.
③SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式:___;H2还原SiHCl3过程中若混入O2,可能引起的后果是___;整个制备过程必须严格控制___.
(3)下列有关硅材料的说法正确的是___(填字母).
A.碳化硅硬度大,可用于生产砂纸、砂轮等
B.氮化硅硬度大、熔点高,可用于制作高温陶瓷和轴承
C.高纯度的二氧化硅可用于制造高性能通讯材料--光导纤维
D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
E.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅.
▼优质解答
答案和解析
(1)高温下,碳和二氧化硅反应生成硅和一氧化碳,反应方程式为:SiO2+2C
Si+2CO↑,高温下,SiHCl3和氢气反应生成硅单质,反应方程式为:SiHCl3+H2
Si+3HCl,
故答案为:SiO2+2C
Si+2CO↑;SiHCl3+H2
Si+3HCl;
(2)①为防止SiHCl3与H2O强烈反应,需要干燥剂干燥氢气,浓硫酸具有吸水性且不和氢气反应,所以装置B中的试剂是浓硫酸;升高温度能使SiHCl3气化,从而使SiHCl3和氢气在D中反应,
故答案为:浓硫酸;使滴入烧瓶中的SiHCl3气化;
②D中发生反应,SiHCl3+H2
Si+3HCl,Si为固态,所以看到的现象是有固体物质生成,SiHCl3与过量的H2在1000℃~1100℃反应制得纯硅,温度太高,普通玻璃管易熔化,
故答案为:有固体物质生成;在此反应温度下,普通玻璃会软化;
③SiHCl3遇水剧烈反应生成H2SiO3、HCl和氢气:SiHCl3+3H2O═H2SiO3+H2↑+3HCl,氢气遇氧气易爆炸,所以整个制备过程必须严格控制无水无氧,
故答案为:SiHCl3+3H2O═H2SiO3+H2↑+3HCl;高温下,H2与O2混合发生爆炸;无水无氧;
(3)A.SiC为原子晶体,硬度大,碳化硅(SiC)俗称金刚砂,常用作砂轮及高温炉的材料,故A正确;
B.Si3N4为原子晶体,硬度大,熔点高,性质稳定,可用于制作高温陶瓷和轴承,故B正确;
C.光导纤维的主要成分是二氧化硅,是利用光的全反射原理,故C正确;
D.普通玻璃的主要成分为Na2SiO3和CaSiO3,它是以石英砂(SiO2)、石灰石(CaCO3)和纯碱(Na2CO3)为主要原料反应制成的,玻璃属于混合物,没有固定的熔点,故D错误;
E.常温下,Si只能与唯一一种酸HF反应,不与HCl反应,故E错误;
故答案为:ABC.
| ||
| ||
故答案为:SiO2+2C
| ||
| ||
(2)①为防止SiHCl3与H2O强烈反应,需要干燥剂干燥氢气,浓硫酸具有吸水性且不和氢气反应,所以装置B中的试剂是浓硫酸;升高温度能使SiHCl3气化,从而使SiHCl3和氢气在D中反应,
故答案为:浓硫酸;使滴入烧瓶中的SiHCl3气化;
②D中发生反应,SiHCl3+H2
| ||
故答案为:有固体物质生成;在此反应温度下,普通玻璃会软化;
③SiHCl3遇水剧烈反应生成H2SiO3、HCl和氢气:SiHCl3+3H2O═H2SiO3+H2↑+3HCl,氢气遇氧气易爆炸,所以整个制备过程必须严格控制无水无氧,
故答案为:SiHCl3+3H2O═H2SiO3+H2↑+3HCl;高温下,H2与O2混合发生爆炸;无水无氧;
(3)A.SiC为原子晶体,硬度大,碳化硅(SiC)俗称金刚砂,常用作砂轮及高温炉的材料,故A正确;
B.Si3N4为原子晶体,硬度大,熔点高,性质稳定,可用于制作高温陶瓷和轴承,故B正确;
C.光导纤维的主要成分是二氧化硅,是利用光的全反射原理,故C正确;
D.普通玻璃的主要成分为Na2SiO3和CaSiO3,它是以石英砂(SiO2)、石灰石(CaCO3)和纯碱(Na2CO3)为主要原料反应制成的,玻璃属于混合物,没有固定的熔点,故D错误;
E.常温下,Si只能与唯一一种酸HF反应,不与HCl反应,故E错误;
故答案为:ABC.
看了硅单质及其化合物应用范围很广....的网友还看了以下:
英语翻译在翻译一份外贸合同时遇到个问题在“合同范围及合同价格”的最后有单独的一句TrainingC 2020-06-05 …
工程索赔的处理原则有( )。A.必须以合同为依据 B.必须及时合理地处理索赔C.必须按国际惯例处理 2020-06-07 …
在编制综合指数时,()。A.指数的分子分母包括的范围必须一致B.若是数量指标综合指数,一般应将同度 2020-06-07 …
工程索赔的处理原则有( )。 A.必须以合同为依据 B.必须及时合理地处理索赔 C.必须按国际 2020-06-07 …
依次填入下面一段文字中横线处的关联词语,恰当的一组是()考试与教学内容涉及的范围必须一致,,考试依 2020-06-27 …
关于集合的题1.已知集合A={x∈R|ax²-3x+2=0},若A是空集,求实属a的取值范围,若△ 2020-07-30 …
索引超出范围.必须为非负值并小于集合大小.参数名:index索引超出范围.必须为非负值并小于集合大小 2020-11-01 …
1{x|x=2n,n∈Z}{x|x=4n+2,n∈Z}2设集合M={a,b},若集合N={x|x是M 2020-11-01 …
英语翻译鲸是海洋中的巨型生物,与海豚同围哺乳动物,(但体型上较海豚大,嘴行较短,前肢进化呈平鳍状,后 2020-11-04 …
2012年9月19日,第67届联合国大会在美国纽约开幕。联合国大会每年召开一次,大会可以就宪章范围内 2021-01-07 …