早教吧作业答案频道 -->化学-->
Cl2及其化合物在生产、生活中具有广泛的用途.25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图一所示.(1)已知HClO的
题目详情
Cl2及其化合物在生产、生活中具有广泛的用途.
25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图一所示.
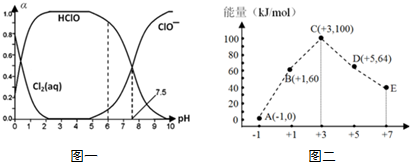
(1)已知HClO的杀菌能力比ClO-强,由图一分析,用氯气处理饮用水时,pH=7.5与pH=6时杀菌效果强的是___.氯气-氯水体系中,存在多个含氯元素的平衡关系,分别用平衡方程式表示为___.
(2)ClO2是一种易爆炸的强氧化性气体,是一种良好的新型消毒剂.工业上可用Cl2氧化NaClO2溶液制取ClO2,该反应的化学方程式为___.最近,科学家又研究出了在酸性溶液中用草酸钠(Na2C2O4)还原氯酸钠制取ClO2的方法,该反应的离子反应方程式为___.此法的优点是___.工业上还可用电解法制备ClO2,在80℃时电解氯化钠溶液得到NaClO3,然后与盐酸反应得到ClO2.电解过程中NaClO3在___极(填“阴”或“阳”)生成,生成ClO3-的电极反应式为___.
(3)一定条件下,在水溶液中 1mol Cl-、1mol ClOx-(x=1、2、3、4)的能量大小与化合价的关系如图二所示.从能量角度看,C、D、E中最不稳定的离子是___(填离子符号).B→A+D反应的热化学方程式为___(用离子符号表示).
25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图一所示.

(1)已知HClO的杀菌能力比ClO-强,由图一分析,用氯气处理饮用水时,pH=7.5与pH=6时杀菌效果强的是___.氯气-氯水体系中,存在多个含氯元素的平衡关系,分别用平衡方程式表示为___.
(2)ClO2是一种易爆炸的强氧化性气体,是一种良好的新型消毒剂.工业上可用Cl2氧化NaClO2溶液制取ClO2,该反应的化学方程式为___.最近,科学家又研究出了在酸性溶液中用草酸钠(Na2C2O4)还原氯酸钠制取ClO2的方法,该反应的离子反应方程式为___.此法的优点是___.工业上还可用电解法制备ClO2,在80℃时电解氯化钠溶液得到NaClO3,然后与盐酸反应得到ClO2.电解过程中NaClO3在___极(填“阴”或“阳”)生成,生成ClO3-的电极反应式为___.
(3)一定条件下,在水溶液中 1mol Cl-、1mol ClOx-(x=1、2、3、4)的能量大小与化合价的关系如图二所示.从能量角度看,C、D、E中最不稳定的离子是___(填离子符号).B→A+D反应的热化学方程式为___(用离子符号表示).
▼优质解答
答案和解析
(1)HClO的杀菌能力比ClO-强,则HClO含量越大其杀菌效果越好,根据图知,pH=6时HClO含量较高,所以pH=6时漂白效果较好,
含氯的物质存在平衡的状态为氯气和水反应,次氯酸电离平衡,液态氯气和气态氯气的平衡等,氯气-氯水体系中,存在多个含氯元素的平衡关系,分别用平衡方程式表示为Cl2(aq)+H2O⇌HClO+H++Cl-; HClO⇌H++ClO-,Cl2(g)⇌Cl2(aq),
故答案为:pH=6时;Cl2(aq)+H2O⇌HClO+H++Cl-,HClO⇌H++ClO-,Cl2(g)⇌Cl2(aq);
(2)ClO2是一种新的消毒剂,工业上可用Cl2氧化NaClO2溶液制取ClO2,结合原则守恒和电子守恒写出该反应的化学方程Cl2+2NaClO2=2NaCl+2ClO2,
在酸性溶液中用草酸钠(Na2C2O4)还原氯酸钠制取ClO2,同时生成二氧化碳,反应的离子方程式为C2O42-+2ClO3-+4H+═2ClO2↑+2CO2↑+2H2O,
电解氯化钠溶液时,阳极上氯离子失电子和水反应生成氯酸根离子和氢离子,电极反应式为Cl--6e-+3 H2O=6H++ClO3-,反应中生成的二氧化碳有稀释作用,大大提高了ClO2生产及储存、运输的安全性,
故答案为:Cl2+2NaClO2═2NaCl+2ClO2;C2O42-+2ClO3-+4H+═2ClO2↑+2CO2↑+2H2O;反应中生成的二氧化碳有稀释作用,大大提高了ClO2生产及储存、运输的安全性;阳; Cl--6e-+3H2O=6H++ClO3-;
(3)图象分析可知,能量越高越活泼,+3价的离子最活泼为ClO2-;
B→A+C,根据转移电子守恒得该反应方程式为3ClO-=ClO3-+2Cl-,反应热=(64kJ/mol+2×0kJ/mol)-3×60kJ/mol=-116kJ/mol,所以该热化学反应方程式为3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-116kJ/mol,
故答案为:ClO2-;3ClO-(aq)=2Cl-(aq)+ClO3-(aq)△H=-116kJ/mol.
含氯的物质存在平衡的状态为氯气和水反应,次氯酸电离平衡,液态氯气和气态氯气的平衡等,氯气-氯水体系中,存在多个含氯元素的平衡关系,分别用平衡方程式表示为Cl2(aq)+H2O⇌HClO+H++Cl-; HClO⇌H++ClO-,Cl2(g)⇌Cl2(aq),
故答案为:pH=6时;Cl2(aq)+H2O⇌HClO+H++Cl-,HClO⇌H++ClO-,Cl2(g)⇌Cl2(aq);
(2)ClO2是一种新的消毒剂,工业上可用Cl2氧化NaClO2溶液制取ClO2,结合原则守恒和电子守恒写出该反应的化学方程Cl2+2NaClO2=2NaCl+2ClO2,
在酸性溶液中用草酸钠(Na2C2O4)还原氯酸钠制取ClO2,同时生成二氧化碳,反应的离子方程式为C2O42-+2ClO3-+4H+═2ClO2↑+2CO2↑+2H2O,
电解氯化钠溶液时,阳极上氯离子失电子和水反应生成氯酸根离子和氢离子,电极反应式为Cl--6e-+3 H2O=6H++ClO3-,反应中生成的二氧化碳有稀释作用,大大提高了ClO2生产及储存、运输的安全性,
故答案为:Cl2+2NaClO2═2NaCl+2ClO2;C2O42-+2ClO3-+4H+═2ClO2↑+2CO2↑+2H2O;反应中生成的二氧化碳有稀释作用,大大提高了ClO2生产及储存、运输的安全性;阳; Cl--6e-+3H2O=6H++ClO3-;
(3)图象分析可知,能量越高越活泼,+3价的离子最活泼为ClO2-;
B→A+C,根据转移电子守恒得该反应方程式为3ClO-=ClO3-+2Cl-,反应热=(64kJ/mol+2×0kJ/mol)-3×60kJ/mol=-116kJ/mol,所以该热化学反应方程式为3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-116kJ/mol,
故答案为:ClO2-;3ClO-(aq)=2Cl-(aq)+ClO3-(aq)△H=-116kJ/mol.
看了Cl2及其化合物在生产、生活中...的网友还看了以下:
已知实系数方程x^2+(m+1)x+m+n+1=0的两实根分别为x1,x2,且0 2020-05-13 …
已知实系数一元二次方程ax²+bx+c=0(A≠0),b²-4ac>0 是它有两个不相等的实数根的 2020-05-16 …
已知实系数一元二次方程x^2+ax+2b=0有两个根,一个根在区间(1,2)内,求点(a,b)对应 2020-05-16 …
已知实系数二次函数f(x)与g(x)满足3f(x)+g(x)=0和f(x)-g(x)=0都有双重实 2020-06-22 …
已知实系数一元二次方程ax2+bx+c=0(a≠0),试判断“b2-4ac=0”是“方程ax2+b 2020-06-22 …
已知实系数一元二次方程ax2+2bx+c=0有两个实根x1、x2,且a>b>c,a+b+c=0,若 2020-07-19 …
请高手指点一下,如何求解积分方程组,其中包含两个积分方程,又有两个未知数,但积分变量的上下限都已知 2020-08-02 …
已知实系数三次多项式函数y=f(x)的最高次项系数为12,其图形与水平线y=25交于相异的三点(0 2020-08-03 …
已知实系数一元二次方程x^2+(1+a)x+a+b+1=0的两个实数根x1、x2,且0 2020-08-03 …
matlab求解带有未知系数的方程,就好比y=x1*x^3+x2*x+x3*x^2+x4,其中x1, 2020-11-04 …