早教吧作业答案频道 -->化学-->
Sn(核电荷数为50)是人类最早使用的元素之一,能形成SnCl2,SnCl4两种氯化物,SnCl2常温下为白色晶体,具有一维链状的聚合结构,气态时以单分子形式存在,而SnCl4常温下为无色液体.白锡
题目详情
Sn(核电荷数为50)是人类最早使用的元素之一,能形成SnCl2,SnCl4两种氯化物,SnCl2常温下为白色晶体,具有一维链状的聚合结构,气态时以单分子形式存在,而SnCl4常温下为无色液体.白锡和灰锡是Sn的两种同素异形体,白锡的晶体结构中Sn原子的配位数为4和6,灰锡的晶体结构与金刚石的晶体结构相似.白锡的密度大于灰锡的密度.
(1)Sn元素外围电子排布式为___.
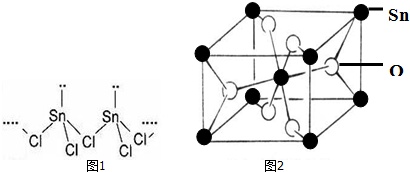
(2)SnCl2的一维链状聚合结构如图1所示,在分子结构中存在的化学键是___.
(3)SnCl4与CCl4中沸点较高的是___.原因是___.
(4)锡的某种氧化物的晶胞如图2,其化学式为___.
(5)解释白锡分子的密度大于灰锡的密度的原因___.

(1)Sn元素外围电子排布式为___.
(2)SnCl2的一维链状聚合结构如图1所示,在分子结构中存在的化学键是___.
(3)SnCl4与CCl4中沸点较高的是___.原因是___.
(4)锡的某种氧化物的晶胞如图2,其化学式为___.
(5)解释白锡分子的密度大于灰锡的密度的原因___.
▼优质解答
答案和解析
(1)Sn属于ⅣA族元素,价电子排布式为ns2np2,位于第5周期,可确定其价电子排布式为:5s25p2,
故答案为:5s25p2;
(2)配位键为Sn提供空轨道,Cl提供孤对电子,根据图1可知形成两条共价键的Cl,其中一条为配位键,配位键表示为由形成两条共价键的Cl指向Sn;
故答案为:共价键、配位键;
(3)SnCl4与CCl4都属于分子晶体,所以相对分子质量较大的分子,范德华力大,熔沸点较高,
故答案为:SnCl4;SnCl4相对分子质量大,范德华力大;
(4)O位于体心和面心,数目为2+4×
=4,Sn位于顶点和体心,数目为8×
+1=2,原子数目比为2:1,化学式为SnO2;
故答案为:SnO2;
(5)白锡的晶体结构中Sn原子的配位数为4和6,灰锡的晶体结构与金刚石的晶体结构相似,配位数为4,前者配位数较大,其空间利用率较大,所以其密度大于灰锡,
故答案为:配位数大,空间利用率大.
故答案为:5s25p2;
(2)配位键为Sn提供空轨道,Cl提供孤对电子,根据图1可知形成两条共价键的Cl,其中一条为配位键,配位键表示为由形成两条共价键的Cl指向Sn;
故答案为:共价键、配位键;
(3)SnCl4与CCl4都属于分子晶体,所以相对分子质量较大的分子,范德华力大,熔沸点较高,
故答案为:SnCl4;SnCl4相对分子质量大,范德华力大;
(4)O位于体心和面心,数目为2+4×
| 1 |
| 2 |
| 1 |
| 8 |
故答案为:SnO2;
(5)白锡的晶体结构中Sn原子的配位数为4和6,灰锡的晶体结构与金刚石的晶体结构相似,配位数为4,前者配位数较大,其空间利用率较大,所以其密度大于灰锡,
故答案为:配位数大,空间利用率大.
看了 Sn(核电荷数为50)是人类...的网友还看了以下:
求数列0,1,1,2,2,3,3,4,4.的前n项和S当n是奇数时.S=2*{[(n-1)/2]* 2020-04-09 …
,;定义在正整数集f(x)对任意m,n,都有f(m+n)=f(m)+f(n)+4(m+n)-2,且 2020-05-13 …
用除了数学归纳法以外的方法证明:2^(n+2)>n^2+3n+4在n≥2时恒成立 2020-05-21 …
我们知道在十进制加法中,逢十进一如9+8=17,也可写成9(10)+8(10)=17(10);在四 2020-05-22 …
线段AB有两个端点一个端点染红色,另一个端点染蓝色.在这个AB线段之间插入n个交点,或然蓝色或然红 2020-07-16 …
对于二项式,4名同学作出了4种判断:①存在n∈N+,展开式中有常数项;②对任意n∈N+,展开式中没 2020-07-31 …
求定积分∫(π/2-π/2)sin4xdx抱歉,问题打错了,是sin∧4x,是四次方,4在n的右上方 2020-10-31 …
数列(1/4+9),(1/2+9/2),(3/4+3),(1+9/4),(5/4+9/5),…中,数 2020-11-06 …
专家请进把一个圆分成n(n>=4)个扇形:S1,S2,...,Sn,现用5种颜色给这n个扇形着色,要 2020-11-13 …
我们可以通过计算求得:1+2+3+...+n=n*(n+1)除以2,其中n是正整数,现在我们来研究一 2020-12-04 …